单选题设NA为阿伏伽德罗常数的数值,下列叙述正确的是()。A 常温下,1L0.1mol/L的NH4NO3溶液中氮原子的数为0.2NAB 1mol羟基中电子数为10NAC 在反应KIO3+6HI=KI+3i2↓+3HO中,每生成3molI2转移的电子数为6NAD 常温常压下,22.4L乙烯中C-H键数为4NA
题目
常温下,1L0.1mol/L的NH4NO3溶液中氮原子的数为0.2NA
1mol羟基中电子数为10NA
在反应KIO3+6HI=KI+3i2↓+3HO中,每生成3molI2转移的电子数为6NA
常温常压下,22.4L乙烯中C-H键数为4NA
相似考题
更多“设NA为阿伏伽德罗常数的数值,下列叙述正确的是()。”相关问题
-
第1题:
下列关于氯的说法正确的是
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.若1735Cl、1737Cl为不同的核素,有不同的化学性质
C.实验室制备Cl2,可用排饱和食盐水集气法收集
D.1.12LCl2含有1.7NA个质子(NA 表示阿伏伽德罗常数)
正确答案:C【解析】Cl2中的氯元素化合价为0处于中间价态,既有氧化性又有还原性,A错误;同位素原子的质子数和电子数分别相等,所以化学性质几乎完全相同,B错误;通过实验室制得的Cl2中含有少量HCl, Cl2在饱和食盐水中溶解度很小,而HCl,易溶,C正确;没有指明气体所处状态, D错误。
-
第2题:
下列有关阿伏加德罗常数NA的表达正确的是( )。
A.它是由意大利科学家阿伏加德罗测出来的
B.它的数值等于6.02×1023
C.它是一个有量纲的常数
D.它的单位是摩尔答案:C解析:单位物质的量的物质含有的粒子数叫阿伏加德罗常数,符号是NA,单位为mol-1,它与0.012kg12C中所含碳原子数相等,大约为6.02×1023,也就是NA约为6.02x1023mol-1。由此判断,B、D两项错误,C项正确。阿伏加德罗常数因阿莫迪欧·阿伏加德罗得名,阿伏加德罗常数的值最早是由约翰·约瑟夫·洛施米特于1865年测出,A项错误。 -
第3题:
ⅣA表示阿伏加德罗常数,则下列说法正确的是( )。 答案:B解析:
答案:B解析: -
第4题:
设NA为阿伏加德罗常数的值,下列说法正确的是()。
A.标准状况下,NA个SO3分子的体积约为22.4 L
B.常温常压下,2 mol氦气所具有的原子数目为2NA
C.1L 0.2 mol·L-1的Na2S溶液中,S2-的数目为0.2NA
D.1mol Cl2与足量的Fe完全反应转移的电子数目为3NA答案:B解析:标准状况下,SO3是固体,不能用标准状况下的气体摩尔体积进行计算,A项错误;因为氦气为单原子分子,所以2 mol氦气含有的原子数为2NA,B项正确;S2-在溶液中发生水解,所以l L 0.2 mol/L的Na2S溶液中S2-的数目小于0.2NA,C项错误;氯气单质是强氧化剂,能将变价金属氧化到高价态,铁与氯气反 应.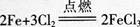 铁从0价变为+3价,l mol铁失去3 mol电子,转移电子数为N=n×NA=3XNA=3NA,但需1.5 m01氯气,所以1mol Cl2与足量的铁反应,电子转移依据氯气计算,转移电子数为2 mol,电子数为N=n×M=2×NA=2NA,D项错误。
铁从0价变为+3价,l mol铁失去3 mol电子,转移电子数为N=n×NA=3XNA=3NA,但需1.5 m01氯气,所以1mol Cl2与足量的铁反应,电子转移依据氯气计算,转移电子数为2 mol,电子数为N=n×M=2×NA=2NA,D项错误。 -
第5题:
NA为阿伏加德罗常数的值。下列说法正确的是( ) 答案:C解析:
答案:C解析:
-
第6题:
设NA为阿伏加德罗常数的数值,下列叙述正确的是( )。 答案:A解析:A项,利用原子守恒,可推知氮原子数为0.2NA,A正确;B项,一个羟基中电子数为9,
答案:A解析:A项,利用原子守恒,可推知氮原子数为0.2NA,A正确;B项,一个羟基中电子数为9,
-
第7题:
在电解含有Ag离子的溶液时.欲使阴极析出1摩尔的银。问需通入的电量是多少?已知每个电子的电荷电量是1.602×10-19库仑,阿伏伽德罗常数NA为6.023×1023
正确答案: 己知1个电子的电量e=1.602×10-19库仑
NA=6.023×1023
Ag+为+1价离子.析出1摩尔银需要1摩尔电子,其电量为:
Q=NA·e=6.023×1023×1.602×10-19
=6.023×1.602×10(23-19)
=9.649×104(库仑)
=96490(库仑)
需要通入电量96490库仑。 -
第8题:
根据Fick的第一扩散定律,下列叙述错误的是()。
- A、扩散速度与扩散面积、浓度差、温度成正比
- B、扩散速度与扩散物质分子半径、液体黏度成反比
- C、扩散系数与扩散物质分子半径成正比
- D、扩散系数与阿伏伽德罗常数有关
- E、扩散系数与克分子气体常数有关
正确答案:C -
第9题:
单选题设阿伏加德罗常数符号为NA,下列说法不正确的为( ).A磷酸的摩尔质量与NA个磷酸分子的质量在数值上相等
BNA个氧分子和NA个氢分子的质量比等于16∶1
C28克氮气所含的原子数目为NA
D在标准状况下,0.5NA个氮气分子所占体积是11.2升
正确答案: C解析:
C项,28g氮气的物质的量为1mol,故氮气分子的数目为NA,一个氮气分子中含有两个氮原子,所以氮原子的数目为2NA. -
第10题:
单选题NA表示阿伏伽德罗常数,下列叙述正确的是()。A等物质的量的N2和CO所含分子数均为NA
B标准状况下,2.24L戊烷所含分子数为0.1NA
C1molNa2O2固体中含离子总数为4NA
D1.7gH2O2中含有的电子数为0.9NA
正确答案: B解析: 1.7gH2O2为0.05mol,每个分子含有18个电子,因此所含电子数为0.9NA。 -
第11题:
多选题设NA表示阿伏加德罗常数,下列叙述中正确的是()A常温常压下,11.2L氧气所含的原子数为NA
B1.8g的NH4+离子中含有的电子数为NA
C常温常压下,48gO3含有的氧原子数为3NA
D2.4g金属镁变为镁离子时失去的电子数为0.1NA
正确答案: C,A解析: 暂无解析 -
第12题:
单选题设N为阿伏加德罗常数的值,下列叙述正确的是()。A1mol氯气参加氧化还原反应,转移的电子数一定为2NA
B25℃时,1LpH=12的Na2CO3溶液中含有Na的数目为0.02NA
C12g石墨和C60的混合物中质子总数一定为6NA
D常温常压下,22.4L乙烯中C-H键数为4NA
正确答案: B解析: A项,1mol氯气参加氧化还原反应,如果氯气全部得电子,转移的电子数一定为2NA,但氯气和水反应时既得电子也失电子,错误;B项,pH=12的Na2CO3溶液中氢氧根是由碳酸根部分水解得到,含有Na+的数目无法判断,错误;C项,12g石墨和C60的混合物,由于基本构成都是碳原子,物质的量是1mol,其中质子总数一定为6NA,正确;D项,常温常压下,22.4L不是1mol,无法判断,错误。故选C。 -
第13题:
阿伏伽德罗常数值6.0221367×1023mol-1为约定真值。 ( )答案:对解析: -
第14题:
NA表示阿伏加德罗常数,下列叙述正确的是( )。A.molFel2与足量氯气反应时转移的电子数为2NA
B.2L0.5mol/L硫酸钾溶液中阴离子所带电荷数为NA。
C.1 molNa202固体中含离子总数为4NA。
D.丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA答案:D解析:
(1 mol Fe2+和2 mol l一)与足量氯气反应时转移的电子数为3NA,A项错误;B项,2 L 0.5 mol/L硫酸钾溶液中含溶质(K2S0。)的物质的量是l mol,所以阴离子S042-的物质的量是l mol,所带电荷数为2NA,B项错误;C项,Na202是由Na+和O22-一构成,所以l mol Na2O2固体中含离子总数是3 mol,含离子总数为3NA。,C项错误;D项,丙烯和环丙烷的最简式都是CH2,则42g混合气体含有3 mol CH2,则氢原子的物质的量是6 mol,个数为6NA,D项正确。故选D。 -
第15题:
设ⅣA为阿伏加德罗常数的值,下列说法正确的是( )。 答案:D解析:
答案:D解析:

-
第16题:
设NA为阿伏加德罗常数的值,下列有关叙述正确的是()。
A.标准状况下,2.24L H2O含有的氧原子数为0.1NA。
B.常温下,14g N2中的氮原子数为0.5NA。
C.2 L 0.5 mol/L亚硫酸溶液中含有的氢离子数为2NA。
D.23gNa在空气中充分燃烧时,转移电子数为NA。答案:D解析:标准状况下H2O为液态,所以标准状况下,2.24 L H2O含有的氧原子数不是0.1NA。常温下,14 g N2中的氮原子数为NA。由于亚硫酸是弱酸,所以2 L 0.5mol/L亚硫酸溶液中含有的氢离子数小于2NA。 -
第17题:
下列化学史实陈述正确的是( )。A、拉瓦锡是最早使用天平的化学家
B、分子概念是由道尔顿最先提出的
C、阿伏加德罗常数是由阿伏加德罗测定出来的
D、苯分子的环状结构是由凯库勒提出的答案:D解析:拉瓦锡建立氧化学说揭开了燃烧现象的本质,他最早运用天平作为研究化学的工具,而埃及人最早使用天平.A项错误。分子概念是由意大利化学家阿伏加德罗最早提出的,B项错误。阿伏加德罗常数是由瑞典化学家J.J.贝采利乌斯测定的,C项错误。苯分子的环状结构是由凯库勒提出的,D项正确。故本题选D。 -
第18题:
设NA为阿伏加德罗常数的值。下列叙述正确的是()。
- A、1mol甲醇中含有C-H键的数目为4NA
- B、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA
- C、标准状况下,2.24L己烷含有分子的数目为0.1NA
- D、常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA
正确答案:D -
第19题:
设氯原子的质量为ag,12C原子的质量为bg,用NA表示阿伏加德罗常数的值,则下列说法正确的是()
- A、氯元素的相对原子质量为12/b
- B、mg该氯原子的物质的量为m/NAmol
- C、该氯原子的摩尔质量是aNA
- D、ng该氯原子所含的电子数是17n/a
正确答案:D -
第20题:
设N为阿伏加德罗常数的值,下列叙述正确的是()。
- A、1mol氯气参加氧化还原反应,转移的电子数一定为2NA
- B、25℃时,1LpH=12的Na2CO3溶液中含有Na的数目为0.02NA
- C、12g石墨和C60的混合物中质子总数一定为6NA
- D、常温常压下,22.4L乙烯中C-H键数为4NA
正确答案:C -
第21题:
单选题设NA为阿伏伽德罗常数的数值,下列叙述正确的是()。A常温下,1L0.1mol/L的NH4NO3溶液中氮原子的数为0.2NA
B1mol羟基中电子数为10NA
C在反应KIO3+6HI=KI+3i2↓+3HO中,每生成3molI2转移的电子数为6NA
D常温常压下,22.4L乙烯中C-H键数为4NA
正确答案: A解析: A项,利用原子守恒,可推知氮原子数为0.2NA,A正确;B项,一个羟基中电子数为9,则1mol羟基中电子数为9NA,故B错;C项,反应KIO3+6HI=KI+3I2↓+3H2O中,生成3molI2时,1molKIO3的I的化合价从+5价变为了0价,6molHI中有5molHI的I的化合价从-1价变为了0价,因此生成3molI2转移电子数为5mol,C错;D项,常温常压下,气体摩尔体积不等于22.4L/mol,则22.4L乙烯不为1mol,D错;故选A。 -
第22题:
单选题设NA为阿伏加德罗常数的值。下列叙述正确的是()。A1mol甲醇中含有C-H键的数目为4NA
B25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA
C标准状况下,2.24L己烷含有分子的数目为0.1NA
D常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA
正确答案: C解析: 1mol甲醇中含有3molC-H键,A项错误;NaOH溶液体积未知无法计算,B项错误;己烷在标准状况下为液体,不适用气体摩尔体积,C项错误;Na2O2与足量H2O反应时,生成0.2molO2,转移0.4mol电子,D项正确。 -
第23题:
单选题若NA表示阿伏伽德罗常数,则下列说法正确的是()。A0.1mol氧气与足量的钠反应得电子数一定为0.4NA
B0.1molNa2CO3固体中共价键数为0.4NA
C0.1mol·L-1FeCl3溶液制成胶体,含有Fe(OH)3胶粒数一定小于0.1NA
D0.1mol甲基中含有电子数为0.7NA
正确答案: D解析: 暂无解析 -
第24题:
单选题设阿佛加德罗常数的符号为NA,下列叙述正确的是()A1摩尔D2O所含质子数为12NA
B10克氖气所含原子数为NA
C0.5摩尔单质铝与足量盐酸反应转移电子数为1.5NA
D标准状况下,升水所含分子数为1/22.4NA
正确答案: A解析: 暂无解析
