单选题已知0.1mol/L某一元弱酸的PH值为3,该弱酸溶液的电离度是:()A 0.01%B 3%C 1%D 0.1%E 以上都不对
题目
0.01%
3%
1%
0.1%
以上都不对
相似考题
参考答案和解析
更多“已知0.1mol/L某一元弱酸的PH值为3,该弱酸溶液的电离度是:()”相关问题
-
第1题:
浓度为0.1mol/L的某弱酸弱碱盐NH4A溶液pH=7.00,则HA的pKa为( )。
(已知:NH3·H2O的Kb=1.8×10-5)
求计算过程
答案:
NH4A在质子论当作两性物质 [H+]=约=[Ka(NH4+) *Ka(HA)]^1/2 [H+]^2 =Ka(NH4+)* Ka(HA) 而Ka(NH4+)=Kw/Kb(NH3) 因此 [H+]^2 =Kw/ Kb(NH3)* Ka(HA) (10^-7)^2=10^-14 /Kb(NH3)* Ka(HA) 即:Ka(HA)=Kb(NH3)=1.8*10^-5。
-
第2题:
有一弱酸HR,在0.1mol·L-1的溶液中有2%电离,试确定该酸在0.05mol·L-1溶液中的电离度()
- A、4.1%
- B、4%
- C、2.8%
- D、3.1%
正确答案:C -
第3题:
缓冲溶液的PH值决定于构成该缓冲溶液的弱酸或弱碱的电离度。
正确答案:错误 -
第4题:
已知0.1mol/L某一元弱酸的PH值为3,该弱酸溶液的电离度是:()
- A、0.01%
- B、3%
- C、1%
- D、0.1%
- E、以上都不对
正确答案:C -
第5题:
某弱酸MOH的Kb=1(×)10-5,则其0.1mol/L溶液的PH值为:()
- A、3.0
- B、5.0
- C、9.0
- D、11.0
- E、12.0
正确答案:D -
第6题:
pH=3,Ka=6.2×10-5的某弱酸溶液,其酸的浓度c(mol/L)为()。
- A、16.1mol/L
- B、0.2mol/L
- C、0.1mol/L
- D、0.02mol/L
正确答案:D -
第7题:
在25℃时,0.1mol·L-1某一元弱酸溶液的电离度为0.2%,则此溶液的OH-浓度为()mol·L-1。
- A、2×10-4
- B、1×10-10
- C、5×10-5
- D、5×10-11
正确答案:D -
第8题:
已知298K时浓度为0.010mol·L-1的某一元弱酸溶液的pH为4.00,则该酸的解离常数等于1.0*10-6;将该酸溶液稀释后,其pH将变大,解离度α将变大,其KaΘ将()。
正确答案:不变 -
第9题:
在弱酸溶液中加水,弱酸的解离度变(),pH值变();在 NH4Cl溶液中,加入HAc,则此盐的水解度变(),pH值变()。
正确答案:大;大;小;小 -
第10题:
某一元弱酸与36.12mL0.100mol·L-1NaOH正好作用完全。然后再加入18.06mL0.100mol·L-1HCl溶液,测得溶液pH=4.92。计算该弱酸的解离常数是()。
正确答案:1.2×10-5 -
第11题:
单选题某一元弱酸溶液的pH=1,该酸溶液的物质的量浓度是( ).A等于0.1mol·L-1
B大于0.1mol·L-1
C小于0.1mol·L-1
D无法判断
正确答案: A解析:
因为该酸是弱酸,在水溶液中不完全电离,因此pH=1的该一元弱酸溶液,其物质的量浓度大于0.1mol/L. -
第12题:
单选题强碱滴定弱酸,理论终点时的溶液pH值与弱酸电离常数的关系是()。A电离常数越小,pH值越低
B电离常数越小,pH值越高
C不论弱酸的电离常数多大,pH值一定
正确答案: B解析: 暂无解析 -
第13题:
已知某一元弱酸的浓度为0.01mol/L,pH=4.55,则其解离常数Ka为( )。A.
B.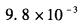
C.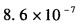
D.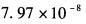 答案:D解析:
答案:D解析: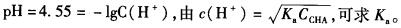
-
第14题:
强碱滴定弱酸,理论终点时的溶液pH值与弱酸电离常数的关系是()。
- A、电离常数越小,pH值越低
- B、电离常数越小,pH值越高
- C、不论弱酸的电离常数多大,pH值一定
正确答案:B -
第15题:
某一元弱酸,浓度为0.1mol·L-1,该溶液的pH=5.15,该一元弱酸的Ka值是()。
- A、5×10-10
- B、4×10-10
- C、5×10-9
- D、4×10-9
正确答案:A -
第16题:
设弱酸HA的电离度为α,0.1mol/L溶液中的氢离子的浓度是:()
- A、αmol/L
- B、0.1αmol/L
- C、0.01αmol/L
- D、0.001αmol/L
- E、0.0001αmol/L
正确答案:B -
第17题:
已知0.1mol/L一元弱酸HR溶液的pH=5.0,则0.1mol/LNaR溶液的pH为()。
- A、9
- B、10
- C、11
- D、12
正确答案:C -
第18题:
已知某一元弱酸的浓度为0.010mol/L,pH=4.55,则其电离常数K为:()
- A、5.8×10-2
- B、9.8×10-3
- C、8.6×10-7
- D、7.9×10-8
正确答案:D -
第19题:
下列*叙述中不正确的是()
- A、对于弱酸溶液,浓度越小,电离度越大,氢离子浓度越大
- B、在多元弱酸的稀溶液中,其酸根的浓度近似等于其最后一级的离解平衡常数
- C、对于弱碱溶液,当加水稀释时,pH值减小
- D、对于弱电解质溶液,同离子效应使其电离度减小,盐效应使其电离度增加
正确答案:A -
第20题:
已知298K时浓度为0.010mol·L-1的某一元弱酸的pH为4.00,则该酸的解离常数为(),当把该酸溶液稀释后,其pH将变(),解离度将变(),其KaΘ()。
正确答案:1.0×10-6;大;大;不变 -
第21题:
0.10mol.L-1的某一有机弱酸的钠盐溶液,其pH=10.0,该弱酸盐的解离度为0.10%。
正确答案:正确 -
第22题:
单选题设弱酸HA的电离度为α,0.1mol/L溶液中的氢离子的浓度是:()Aαmol/L
B0.1αmol/L
C0.01αmol/L
D0.001αmol/L
E0.0001αmol/L
正确答案: A解析: 暂无解析 -
第23题:
单选题已知某一元弱酸的浓度为0.010mol/L,pH=4.55,则其电离常数Ka为()A5.8×10-2
B9.8×10-3
C8.6×10-7
D7.9×10-8
正确答案: A解析: 暂无解析
