下列键能大小顺序中正确的是()A、O2+<O2<O2-B、O2-<O2<O2+C、O2<O2-<O2+
题目
下列键能大小顺序中正确的是()
- A、O2+<O2<O2-
- B、O2-<O2<O2+
- C、O2<O2-<O2+
相似考题
更多“下列键能大小顺序中正确的是()”相关问题
-
第1题:
根据价键理论,下列哪一种说法是正确的
A、键能愈强,键长愈长,愈稳定
B、键能愈弱,键长愈长,愈稳定
C、键能愈强,键长愈长,愈不稳定
D、键能愈弱,键长愈短,愈稳定
E、键能愈强,键长愈短,愈稳定
参考答案:E
-
第2题:
下列化学物质毒性大小比较正确的顺序是 ( )
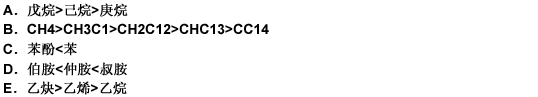 正确答案:E
正确答案:E
-
第3题:
下列晶格能大小顺序中正确的是哪个?()
- A、CaO>KCl>MgO>NaCl
- B、NaCl>KCl>RbCl>SrO
- C、MgO>RbCl>SrO>BaO
- D、MgO>NaCl>KCl>RbCl
正确答案:D -
第4题:
在下列元素电负性大小顺序中,正确的是哪一组?()
- A、B>Al>Be≈Mg
- B、B>Be≈Al>Mg
- C、B≈Al
- D、Be>B>Al>Mg
正确答案:B -
第5题:
下列哪些操作可以实现在打开的多个文件中切换()
- A、在“窗口”菜单中单击要切换的文件名
- B、单击任务栏上的任务图标
- C、按组合键[Ctrl]+F6键顺序切换
- D、按组合键[Shift]+F6键顺序切换
- E、按组合键[Alt]+F6键顺序切换
正确答案:A,B,C -
第6题:
关于共价键的说法,下述说法正确的是()
- A、一般来说σ键键能小于π键键能;
- B、原子形成共价键的数目等于基态原子的未成对电子数
- C、相同原子间的双键键能是单键键能的两倍
- D、所有不同原子间的键至少具有弱极性
正确答案:D -
第7题:
在下列操作中,能按顺序切换输入法的操作是()
- A、用CTRL+shift键
- B、用鼠标右键双击输入方式切换按钮
- C、用shift+空格
- D、用ALT+shift键
正确答案:A -
第8题:
下列原子半径大小顺序中正确的是()
- A、Be<Na<Mg
- B、Be<Mg<Na
- C、Na<Be<Mg
正确答案:B -
第9题:
下列操作中,能实现全角与半角切换的功能键是()
- A、Ctrl+Shift键
- B、Ctrl+空格键
- C、Alt+Shift键
- D、Shift+空格键
正确答案:D -
第10题:
单选题在下列CaO、MgO、NaF晶格能大小的顺序中,正确的是哪一组?()AMgO>CaO>NaF
BNaF>CaO>MgO
CCaO>MgO>NaF
DNaF>MgO>CaO
正确答案: A解析: 暂无解析 -
第11题:
单选题在下列元素电负性大小顺序中,正确的是哪一组()?AB>Al>Be≈Mg
BB>Be≈Al>Mg
CB≈Al
DBe>B>Al>Mg
正确答案: B解析: 暂无解析 -
第12题:
单选题下列晶格能大小顺序正确的是( )。ACaO>KCl>MgO>NaCl
BNaCl>KCl>RbCl>SrO
CMgO>RbCl>SrO>BaO
DMgO>NaCl>KCl>RbCl
正确答案: D解析:
对晶体构型相同的离子化合物,离子电荷数越多,荷间距越短,晶格能就越大。 -
第13题:
根据价键理论,说法正确的是
A、键能愈强,键长愈长,愈稳定
B、键能与键长无关
C、键能愈强,键长愈短,愈稳定
D、键能愈弱,键长愈长,愈稳定
E、键能愈弱,键长愈短,愈稳定
参考答案:C
-
第14题:
在下列CaO、MgO、NaF晶格能大小的顺序中,正确的是哪一组?A. MgO>CaO>NaF C. CaO>MgO>NaF
B. NaF>CaO>MgO D. NaF>MgO>CaO答案:A解析:提示:影响晶格能的因素主要是离子电荷与离子半径。它们的关系可粗略表示为
在MgO和CaO中,Z+ 、Z- 、r-都相同,不同的是r+ ,由于rMg2+ 2+,所以晶格能: MgO>CaO。在CaO和NaF中,Na与Ca在周期表中处于对角线位置,它们的半径近似相等。虽然ro2-略大于rF- ,但决定晶格能大小的主要因素仍为Z+和Z_。在CaO中Z+与均高于NaF中的Z+与Z- ,所以晶格能CaO>NaF。 -
第15题:
在虚电路操作方式下,下列描述中错误的是()。
- A、能保证每个分组正确到达,且分组顺序发生了变化
- B、能保证每个分组正确到达,且分组顺序不发生变化
- C、不能保证每个分组正确到达,且分组顺序发生了变化
- D、不能保证每个分组正确到达,有的分组会丢失
正确答案:A,C,D -
第16题:
在下列CaO、MgO、NaF晶格能大小的顺序中,正确的是哪一组?()
- A、MgO>CaO>NaF
- B、NaF>CaO>MgO
- C、CaO>MgO>NaF
- D、NaF>MgO>CaO
正确答案:A -
第17题:
下列各对元素中,第一电离势大小顺序正确的是()
- A、Cs>Au
- B、Zn>Cu
- C、S>P
- D、Rb>Sr
- E、Mg>Al
正确答案:B,E -
第18题:
下列晶格能大小顺序中正确的是()
- A、CaO>KCl>MgO>NaCl
- B、NaCl>KCl>RbCl>SrO
- C、MgO>RbCl>SrO>BaO
- D、MgO>NaCl>KCl>RbCl
正确答案:D -
第19题:
解释“C-X键的极性大小顺序为C-F>C-Cl>C-Br>C-I,而C-X键的极化度大小顺序为C-I>C-Br>C-Cl>C-F?
正确答案:键的极性,决定于两个成键原子的电负性,电负性相差越大,键的极性就越大。由于卤原子的电负性大小顺序为F>Cl>Br>I,所以,C-X键的极性大小顺序为C-F>C-Cl>C-Br>C-I;键的极化度与成键原子的体积有关,即与原子核对最外层电子云吸引能力有关。当原子核对最外层电子云吸引能力愈强时,键的极化越困难;反之,则键的极化越容易。键极化的难易程度称为极化度。在同一族中,原子半径越大,最外层电子云受原子核的束缚力越小,极化度越大。由于卤原子的半径大小顺序为I>Br>Cl>F,所以,C-X键的极化度大小顺序为:C-I>C-Br>C-Cl>C-F。 -
第20题:
下列物质晶格能大小顺序中正确的是()
- A、MgO>CaO>NaF
- B、CaO>MgO>NaF
- C、NaF>MgO>CaO
- D、NaF>CaO>MgO
正确答案:A -
第21题:
下列对 -淀粉酶的叙述,不正确的是()
- A、对热不稳定
- B、对酸不稳定
- C、能水解淀粉中的α-1,4糖苷键
- D、能水解淀粉中的α-1,6糖苷键
正确答案:A,D -
第22题:
多选题下列对 -淀粉酶的叙述,不正确的是()A对热不稳定
B对酸不稳定
C能水解淀粉中的α-1,4糖苷键
D能水解淀粉中的α-1,6糖苷键
正确答案: B,C解析: 暂无解析 -
第23题:
单选题在下列元素电负性大小顺序中,正确的是哪一组?()AB>Al>Be≈Mg
BB>Be≈Al>Mg
CB≈Al
DBe>B>Al>Mg
正确答案: B解析: 暂无解析
