等重的葡萄糖及甘油分别溶于100g水中,所得溶液的凝固点、沸点、渗透压是否相同,为什么?
题目
等重的葡萄糖及甘油分别溶于100g水中,所得溶液的凝固点、沸点、渗透压是否相同,为什么?
相似考题
参考答案和解析
更多“等重的葡萄糖及甘油分别溶于100g水中,所得溶液的凝固点、沸点、”相关问题
-
第1题:
2.76g甘油溶于200g水中得到一种溶液,测得该溶液的凝固点为-0.279℃,水的Kfp=1.86K·kg/mol。据此求出该甘油的摩尔质量是( )。A.860g/mol
B.920g/mol
C.900g/mol
D.940g/mol答案:B解析:根据公式Kfp·m=△Tfp进行计算 -
第2题:
在20℃时,将15.0g葡萄糖(C6H12O6)溶于200g水中,该溶液的冰点(Kfp=1.86℃)、正常沸点(Kbp=0.52℃)、渗透压(设M=m)分别是( )。 答案:C解析:
答案:C解析:
-
第3题:
相同质量的葡萄糖和甘油分别溶于l00g水中,所得到的两个溶液的凝固点相同。
正确答案:错误 -
第4题:
为防止水箱结冰,可加入甘油以降低其凝固点。如需使凝固点降到-3.15℃,在100g水中应加入甘油()克。(已知水的凝固点下降常数1.86℃•kg•mol-1)
- A、5
- B、10
- C、15
- D、20
正确答案:C -
第5题:
真空式除碳器是利用真空泵或喷射器的上部抽真空,使水达到(),出去溶于水中的气体。
- A、凝固点
- B、沸点
- C、熔点
- D、冰点
正确答案:B -
第6题:
1.84g氯化汞溶于100g水,测得该水溶液的凝固点为-0.126℃,由计算结果说明氯化汞在水溶液中的存在形式。(氯化汞摩尔质量为272g•mol-1)
正确答案:以HgCl2共价分子形式存在 -
第7题:
称取某一有机化合物9.00克溶于200g水中,测其溶液的凝固点为-0.186℃,该有机物的摩尔质量为(),此有机物溶液的沸点为()K。
正确答案:450;373.2 -
第8题:
在20℃时,将7.50g葡萄糖(C6H12O6)溶于100g水中。该溶液的渗透压为:()
- A、69.3Pa
- B、1.02×103kPa
- C、1.02×103Pa
- D、69.3kPa
正确答案:C -
第9题:
NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?
正确答案: NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。因为两者溶液中均为Na+,K+,Br-,Cl-离子各1mol。 -
第10题:
稀溶液凝固点下降公式要求();而沸点上升公式则要求()。
正确答案:溶质B不与溶剂A形成固熔体;溶质是非挥发性的 -
第11题:
单选题2.60克尿素[CO(NH2)2]溶于50.0克水中,此溶液的凝固点(kfp=1.86)和沸点(kbp=0.52)分别为(尿素的分子量M=60)( )。A1.61℃和99.55℃
B-1.61℃和99.55℃
C1.61℃和100.45℃
D-1.61℃和100.45℃
正确答案: B解析:
尿素的摩尔质量为60g·mol-1,尿素的物质的量n=2.6/60=0.043mol,则:
①质量摩尔浓度m=(0.043/50)×1000=0.86mol•kg-1
凝固点降低度ΔTfp=kfp·m=1.86×0.86=1.60℃;
则此溶液的凝固点为:0-1.60=-1.60℃。
②沸点升高度ΔTbp=kbp·m=0.52×0.86=0.45℃;
则此溶液的沸点为:100+0.45=100.45℃。 -
第12题:
单选题在20℃时,将7.50g葡萄糖(C6H12O6)溶于100g水中。该溶液的渗透压为()A69.3Pa
B1.02×103kPa
C1.02×103Pa
D69.3kPa
正确答案: C解析: 暂无解析 -
第13题:
在20°C时,将7.50g葡萄糖(C6H1206)溶于100g水中。该溶液的渗透压为:A. 69. 3Pa
B. 1. 02X103kPa
C. 1.02X103Pa
D. 69. 3kPa答案:C解析: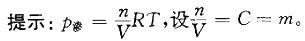
-
第14题:
凝固点差别很大(),沸点范围为常温到()摄氏度以上,可溶于多种(),不溶于水,但可与水形成乳状液。
正确答案:30~-60摄氏度;500;有机溶剂 -
第15题:
将蔗糖溶于纯水中形成稀溶液,与纯水比较,其沸点()。
- A、降低
- B、升高
- C、无影响
- D、不能确定
正确答案:B -
第16题:
真空式除碳器是利用真空泵或喷射器从除碳器的上部抽真空,使水达到(),除去溶于水中的气体。
- A、凝固点
- B、沸点
- C、熔点
- D、冰点
正确答案:B -
第17题:
稀溶液依数性的本质是:()
- A、渗透压
- B、沸点升高
- C、蒸气压下降
- D、凝固点下降
- E、沸点升高和凝固点下降
正确答案:C -
第18题:
两种溶液,一是7.5 g 尿素溶于200g水中配成,另一为11.3g 某未知难挥发非电解质溶于50.0g水中配成,二者沸点相同,则此未知物的摩尔质量为()。
正确答案:361 -
第19题:
分别在四杯100毫升水中加入5克乙二酸、甘油、季戊四醇、蔗糖形成四种溶液,则这四种溶液的凝固点()。
- A、都相同
- B、加蔗糖的低
- C、加乙二酸的低
- D、无法判断
正确答案:C -
第20题:
在纯水、以及浓度均为0.1mol/kg的KCl、K2SO4、蔗糖、乙醇、NAAC溶液中,沸点最高的是(),沸点最低的是(),凝固点最高的是(),凝固点最低的是()。
正确答案:K2SO4溶液;乙醇溶液;纯水;K2SO4溶液 -
第21题:
0.005molkg-1的硫酸钾水溶液其沸点较纯水的沸点升高了0.0073℃。已知水的质量摩尔凝固点降低常数Kf和沸点升高常数Kb分别为1.86和0.52,则该溶液的凝固点(以℃表示)是()
- A、-0.0018
- B、5.222
- C、-0.0261
- D、-0.0020
正确答案:C -
第22题:
单选题称取相同质量的两种非电解质A和B分别溶于相同质量的水中,测得A溶液的凝固点比B溶液的高,则MA与MB的关系是()。AMA>MB
BMA<MB
CMA=MB
D无法确定
正确答案: B解析: 暂无解析 -
第23题:
单选题溶质溶于溶剂之后将会引起()。A沸点降低
B凝固点升高
C蒸气压下降
D蒸气压、沸点、凝固点都不变
正确答案: D解析: 暂无解析
