已知氢电极Pt∣H+(c)∣H2(100kPa)的电极电势为-0.0592V,则c(H+)应为A.1 mol·L-1B.0.1 mol·L-1C.0.01 mol·L-1D.10 mol·L-1
题目
已知氢电极Pt∣H+(c)∣H2(100kPa)的电极电势为-0.0592V,则c(H+)应为
A.1 mol·L-1
B.0.1 mol·L-1
C.0.01 mol·L-1
D.10 mol·L-1
相似考题
更多“已知氢电极Pt∣H+(c)∣H2(100kPa)的电极电势为-0.0592V,则c(H+)应为”相关问题
-
第1题:
标准氢电极的电极电位为()伏,测定条件是[H+]=mol/L,pH2=()MPa。参考答案: 0;1;0.101。
-
第2题:
标准电极电势是:
(A)电极相对于标准氢电极的电极电势
(B)在标准状态下,电极相对于标准氢电扱的电极电势
(C)在任何条件下,可以直接使用的电极电势
(D)与物质的性质无关的电极电势答案:B解析:点评:概念题。
-
第3题:
有关标准氢电极的叙述,不正确的是()
- A、标准氢电极是指将吸附纯氢气(1.01×105Pa)达饱和的镀铂黑的铂片浸在H+浓度为1mol·L-1的酸性溶液中组成的电极.
- B、使用标准氢电极可以测定所有金属的标准电极电势.
- C、H2分压为1.01×105Pa,H+的浓度已知但不是1mol·L-1的氢电极也可用来测定其它电极电势.
- D、任何一个电极的电势绝对值都无法测得,电极电势是指定标准氢电极的电势为0而测出的相对电势
正确答案:B -
第4题:
(2012)在铜锌原电池中,将铜电极的c(H+)由1mol/L增加到2mol/L,则铜电极的电极电势:()
- A、变大
- B、变小
- C、无变化
- D、无法确定
正确答案:C -
第5题:
将反应:Cu2+(c1)+H2(g)=Cu(s)+2H+(c2)设计组成电池,其正确的电池符号书写形式是()
- A、(-)Pt│Cu2+(c1)丨Cu(s)‖H+(c2)│H2(kPa)(+)
- B、(-)Cu(s)│Cu2+(c1)‖H+(c2)│H2(kPa)(+)
- C、(-)H2(kPa)│H+(c2)‖Cu2+(c1)丨Cu(s)│Pt(+)
- D、(-)Pt│H2(kPa)│H+(c2)‖Cu2+(c1)│Cu(s)(+)
正确答案:D -
第6题:
已知氯电极的标准电势为1.358V,当氯离子浓度为0.1mol·L-1、氯气分压为0.1×100kPa时,该电极的电极电势为()。
- A、1.358V
- B、1.328V
- C、1.388V
- D、1.417V
正确答案:C -
第7题:
在酸性溶液中Fe易腐蚀是因为()
- A、Fe2+/Fe的标准电极电势下降
- B、Fe3+/Fe2+的标准电极电势上升
- C、EHH/H的值因〔H+〕增大而上升
- D、EH/H的值下降
正确答案:C -
第8题:
电池Pt|H2(0.1p9)|H+(aH+=1)||Cu2+|Cu的电动势()
- A、是铜电极的电极电势
- B、随aH+的增大而增大
- C、不因温度改变而改变
- D、不因向Cu2+溶液中加入NaCl而改变
正确答案:B -
第9题:
金属活性排在H2之前的金属离子,如Na+能优先于H+在汞阴极上析出,这是由于:()
- A、φθ(Na+/Na)< φθ(H+/H2)
- B、η(Na)< η(H2)
- C、φ(Na+/Na)< φ(H+/H2)
- D、H2在汞上析出有很大的超电势,以至于φ(Na+/Na)>φ(H+/H2)
正确答案:D -
第10题:
单选题在铜锌原电池中,将铜电极的c(H+)由1mol/L增加到2mol/L,则铜电极的电极电势()。A变大
B变小
C无变化
D无法确定
正确答案: D解析: 暂无解析 -
第11题:
单选题已知氯电极的标准电极电势为1.358V,当氯离子浓度为0.1mol/L,氯气浓度为0.1×100kPa时,该电极的电极电势为()V。A1.358
B1.328
C1.388
D1.417
正确答案: B解析: 暂无解析 -
第12题:
单选题假设规定标准氢电极的电极电势φθ(H+/H2)=1V,则测得下列原电池:(-)Zn|Zn2+(1mol·dm-3)||H+(1mol·dm-3)|H2(pθ)(Pt)(+)的标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)的数值变化为()A标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)各增加1V
B标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)各减少1V
C标准电动势Eθ不变,锌标准电极电势φθ(Zn2+/Zn)增加1V
D标准电动势Eθ不变,锌标准电极电势φθ(Zn2+/Zn)减少1V
E标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)均不变
正确答案: E解析: 暂无解析 -
第13题:
下列各电对的电极电势与H+浓度有关的是( )。A、 Zn2+/Zn
B、 Br2/Br-
C、 AgI/Ag
D、 MnO-4/Mn2+答案:D解析:离子的浓度对电极电势有影响,四个选项的电极反应分别为:
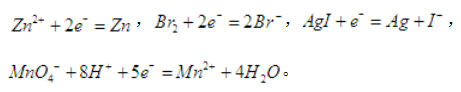
故只有D项当H+浓度变化时,电极电势才会有变化,H+浓度升高,电极电势升高。 -
第14题:
己知氯电极的标准电极电势为1.358V,当氯离子浓度为0.1mol/L,氯气浓度为 0.1×100kPa时,该电极的电极电势为( )V。
A. 1.358 B. 1.328 C. 1.388 D. 1.417答案:C解析:
-
第15题:
将氢电极(p(H2)=100kPa)插入纯水中,与标准氢电极组成一个原电池,则EMF=()
- A、0.414V
- B、-0.414V
- C、0V
- D、0.828V
正确答案:A -
第16题:
今有电池:(-)Pt,H2(g)∣H+‖Cu+∣Cu(+),要增加电池电动势的办法是()
- A、负极加大[H+]
- B、负极降低H2气分压
- C、正极加大[Cu+]
- D、正极加入氨水
正确答案:C -
第17题:
在Pt|H2(101.325Pa)/ H+(1mol.L-1) || Fe3+(1mol.L-1),Fe2+(1mol.L-1)| Pt 电池中,电子转移是()
- A、Fe2+→Fe3+
- B、H2→Fe3+
- C、H2→H+
- D、Fe2+→H+
正确答案:B -
第18题:
(2006)标准电极电势是:()
- A、电极相对于标准氢电极的电极电势
- B、在标准状态下,电极相对于标准氢电极的电极电势
- C、在任何条件下,可以直接使用的电极电势
- D、与物质的性质无关的电极电势
正确答案:B -
第19题:
按照电极电势的定义,将标准氢电极与待测电极组成电池,若待测电极发生氧化作用,则电极电势φ()0;该电极是电池的()极。
正确答案:<;负极 -
第20题:
在还原性酸性溶液中,Zn的腐蚀速度较Fe为小,其原因是:()
- A、φ(Zn2+/Zn)(平) < φ(Fe2+/Fe)(平)
- B、φ(Zn2+/Zn) < φ(Fe2+/Fe)
- C、φ(H+/H2)(平,Zn) < φ(H+/H2)(平,Fe)
- D、φ(H+/H2)(Zn) < φ (H+/H2)(Fe)
正确答案:D -
第21题:
已知Tl3+,Tl+∣Pt的标准电极电势EθTl3+,Tl+Pt=1.250V,Tl+∣Tl的标准电极电势EθTl+|Tl=-0.336V,则Tl3+∣Tl的标准电极电势EθTl3+,Tl+pt为 ()。
- A、1.586V
- B、0.914V
- C、0.721V
- D、0.305V
正确答案:C -
第22题:
单选题已知氯电极的标准电极电势为1.358V,当氯离子浓度为0.1mol/L,氯气浓度为0.1×100kPa时,该电极的电极电势为( )A1.358V
B1.328V
C1.388V
D1.417V
正确答案: D解析: -
第23题:
单选题标准氢电极指的是()APt ∣ H2(PH2 = Pθ)∣OH-(a=1)
BPt ∣ H2(PH2=Pθ)∣H+(a=1)
CPt ∣ H2(PH2=Pθ)∣H+(a=10-7)
DPt ∣ H2(PH2=Pθ)∣OH+(a=10-7)
正确答案: C解析: 暂无解析 -
第24题:
填空题25℃条件下,镀了铂黑的Pt浸在压力101325Pa(1atm)的H2气氛下的H+活度为1mol/L的HCl溶液中构成的电极系统称为()。正确答案: 氢标准电极解析: 暂无解析
