(2)求:所加稀盐酸的溶质质量分数和反应后所得溶液中溶质的质量。(写出计算过程)
题目
(2)求:所加稀盐酸的溶质质量分数和反应后所得溶液中溶质的质量。(写出计算过程)
相似考题
更多“(2)求:所加稀盐酸的溶质质量分数和反应后所得溶液中溶质的质量。(写出计算过程) ”相关问题
-
第1题:
在稀溶液凝固点降低公式△Tf=kf²m中,m所代表的是溶液中。()A、溶质的质量摩尔浓度
B、溶质的摩尔分数
C、溶剂的摩尔分数
D、溶质的体积摩尔浓度
参考答案:A
-
第2题:
(10分)⑴利用如图所示装置可测定空气中氧气的含量。
①实验现象,红色物质逐渐变成 。
②反应的化学方程式为 。
③停止加热冷却至室温,注射器内气体的体积大约减少了 。
④实验结论 。
⑵50g溶质质量分数为7.3%的稀盐酸与50g一定溶质质量分数的氢氧化钠溶液恰好完全反应,求反应后所得溶液溶质质量分数。
正确答案:
14、(10分)⑴
①黑色 ②2 Cu+ O2 ==() 2CuO
③约1/5
④空气中氧气的体积分数大约为1/5
⑵解:设生成的氯化钠的质量为x
HCl+NaOH=NaCl+H2O
36.5 58.5
50g×7.3% x
x=5.85g
所得氯化钠溶液中氯化钠的质量分数为:5.85%
答:略
-
第3题:
现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2 = CaCO3↓+2NaCl)。反应时CaCl2溶液与沉淀的质量关系如图所示。请解决以下问题: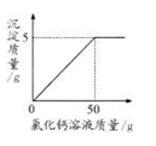
(1)计算样品中NaOH的质量;
(2)计算所加CaCl2溶液的溶质质量分数;
(3)恰好完全反应时烧杯中溶液的pH______7(选填“>”、“<”或“=”)答案:解析:(1)解:设样品中碳酸钠的质量为x,加入的氯化钙溶液中的溶质质量为y
Na2C03+CaCl2=CaC03↓ +2NaCl
106 111 100
x Y 5 g
106/100=x/5g
x=5.3 g
该样品中NaOH的质量为l0 g-5.3 g=4.7 g
(2)111/y=100/5g
y= 5.55 g
所加CaCl2溶液的溶质质量分数=5.55g/50g×l00%=11.1%
答:样品中NaOH的质量为4.7 g,所加CaCl2溶液的溶质质量分数为ll.1%
(3) > -
第4题:
某温度时,蒸干35g氯化钾溶液,得到7g氯化钾,求该溶液中溶质的质量分数。
20% -
第5题:
为测定某铜锌合金中的铜的质量分数,某校化学兴趣小组用该合金与稀硫酸反应,进行了三次实验。所有的相关数据记录见下表(实验误差忽略不计);
(1)计算该合金中铜的质量分数;
(2)求第三次实验所得溶液中溶质的质量分数。答案:解析:
