一物质系统从外界吸收一定的热量,则系统的温度有何变化? A.系统的温度一定升高 B.系统的温度一定降低 C.系统的温度一定保持不变 D.系统的温度可能升高,也可能降低或保持不变
题目
B.系统的温度一定降低
C.系统的温度一定保持不变
D.系统的温度可能升高,也可能降低或保持不变
相似考题
参考答案和解析
更多“一物质系统从外界吸收一定的热量,则系统的温度有何变化? ”相关问题
-
第1题:
一卡诺致冷机在工作时,低温热源温度为-10℃,高温热源温度为11℃。若在一次循环中,外界对系统做功1000J,则系统从低温热源吸收的热量应为( )。A.-476J
B.524J
C.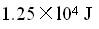
D.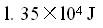 答案:C解析:
答案:C解析: -
第2题:
一个物质系统从外界吸收一定的热量,则内能变化为( )。A.系统的内能一定增加
B.系统的内能一定减少
C.系统的内能一定保持不变
D.系统的内能可能增加,也可能减少或保持不变答案:D解析:热力学第一定律:Q=W+ΔE,吸收的热量可能全用于做功,也可分配为内能,甚至耗散内能做功,故系统的内能可能增加,也可能减少或保持不变。 -
第3题:
开口系统是指()的热力系统。
- A、具有活动边界
- B、与外界有功量交换
- C、与外界有热量交换
- D、与外界有物质交换
正确答案:D -
第4题:
可逆过程中系统的()变化是系统和外界传递热量的标志。
- A、内能
- B、焓
- C、熵
- D、温度
正确答案:C -
第5题:
一物质系统从外界吸收一定的热量,则()。
- A、系统的温度一定保持不变
- B、系统的温度一定降低
- C、系统的温度可能升高,也可降低或保持不变
- D、系统的温度一定升高
正确答案:C -
第6题:
热力学第一定律表明:()
- A、系统对外做的功不可能大于系统从外界吸收的热量
- B、系统内能的增量等于系统从外界吸收的热量
- C、不可能存在这样的循环过程,在此循环过程中,外界对系统做的功不等于系统传给外界的热量.
- D、热机的效率不可能等于
正确答案:C -
第7题:
水蒸气凝结有以下()特点。
- A、一定压力下的水蒸气,必须降到该压力所对应的凝结温度才开始凝结成液体。
- B、压力降低,凝结温度随之降低,反之,则凝结温度升高。
- C、在凝结温度下,水从水蒸气中不断吸收热量,则水蒸气可以不断凝结成水。
- D、在凝结温度下,水从水蒸气中不断吸收热量,并保持温度不变。
正确答案:A,B,C,D -
第8题:
单选题开口系统是指()的系统。A与外界有物质交换
B与外界有热量交换
C与外界有物质交换没有热量交换
D与外界有功的交换
正确答案: D解析: 暂无解析 -
第9题:
单选题封闭系统是指()的系统。A与外界没有物质交换
B与外界没有热量交换
C与外界既没有物质交换也没有热量交换
D与外界没有功的交换
正确答案: B解析: 暂无解析 -
第10题:
单选题一物质系统从外界吸收一定的热量,则系统的温度有何变化?()A系统的温度一定升高
B系统的温度一定降低
C系统的温度一定保持不变
D系统的温度可能升高,也可能降低或保持不变
正确答案: D解析: 暂无解析 -
第11题:
单选题一物质系统从外界吸收一定的热量,则()。A系统的温度一定保持不变
B系统的温度一定降低
C系统的温度可能升高,也可降低或保持不变
D系统的温度一定升高
正确答案: B解析: 暂无解析 -
第12题:
单选题当系统从热源吸收一定数量的热量时,工质绝对温度(),则系统熵的变化(),热量转变为功的程度()。A越高/越小/越大
B越高/越大/越大
C越低/越小/越小
D越低/越小/越大
正确答案: C解析: 暂无解析 -
第13题:
一物质系统从外界吸收一定的热量,则系统的温度有何变化?A.系统的温度一定升高
B.系统的温度一定降低
C.系统的温度一定保持不变
D.系统的温度可能升高,也可能降低或保持不变答案:D解析: -
第14题:
热力学第一定律的解析式q=Au+w中,如果q是负数,则表明()。
- A、工质接受了外界压力
- B、工质向外界传出热量
- C、工质从外界吸收热量
- D、工质的内能增加了
正确答案:B -
第15题:
关于物质的显热,说法正确的是()。
- A、物质没有相变化,升温时吸收的热量
- B、物质没有相变化,降温时放出的热量
- C、物质温度无变化,汽化时吸收的热量
- D、物质温度无变化,冷凝时放出的热量
正确答案:A,B -
第16题:
关于物质的潜热,说法正确的是()。
- A、物质没有相变化,升温时吸收的热量
- B、物质没有相变化,降温时放出的热量
- C、物质温度无变化,汽化时吸收的热量
- D、物质温度无变化,冷凝时放出的热量
正确答案:C,D -
第17题:
系统经历一个可逆定温过程时,既然温度没有变化,所以不能与外界交换热量。
正确答案:错误 -
第18题:
一定量的气体,从始态A变化到终态B,系统吸收100J的热量,对外作功200J, 这不符合热力学第一定律。
正确答案:错误 -
第19题:
根据热力学第一定律,因为能量不会无中生有,所以一个系统如要对外做功,必须从外界吸收热量。
正确答案:错误 -
第20题:
单选题有一闭口系统沿过程a从状态1变化到状态2,又从状态2沿另一过程b回到状态1。如果已知系统在1-a-2过程中向外界吸收热量10kJ,外界在2-b-1过程中对系统做压缩功8kJ而系统向外界放热9kJ,那么,系统在1-a-2过程中对外界做功为( )。A8kJ
B11kJ
C9kJ
D6kJ
正确答案: D解析:
热力学第一定律基本表达式为:Q=ΔU+W。由题意可得,2-b-1过程中,做功W2b1=-8kJ,热量Q2b1=-9kJ,则热力学能ΔU2b1=Q2b1-W2b1=-9-(-8)=-1kJ。热力学能ΔU为状态参数,只与初末状态,因此ΔU1a2+ΔU2b1=0,即ΔU1a2=-ΔU2b1=1kJ。1-a-2过程中,热量Q1a2=10kJ,则做功W1a2=Q1a2-ΔU1a2=10-1=9kJ,即表示系统对外界做功9kJ。 -
第21题:
单选题热力学第一定律表明()A系统对外做的功不可能大于系统从外界吸收的热量
B系统内能的增量等于系统从外界吸收的热量
C不可能存在这样的循环过程,在此循环过程中,外界对系统做的功不等于系统传给外界的热量
D热机的效率不可能等于1
正确答案: C解析: 暂无解析 -
第22题:
单选题当系统从热源吸收一定数量的热量时,工质绝对温度越高,则系统熵的变化越小,热量转变为功的程度()。A越小
B越大
C不受影响
D均不对
正确答案: A解析: 暂无解析 -
第23题:
单选题当系统从热源吸收一定数量的热量时,工质绝对温度(),则系统熵的变化越大,热量转变为功的程度()。A越低/越大
B越高/越大
C越低/越小
D越高/越小
正确答案: A解析: 暂无解析 -
第24题:
单选题空调制冷系统的制冷过程是利用制冷剂()。A液化吸收热量
B气化吸收热量
C温度变化吸收热量
D沸腾吸收热量
正确答案: C解析: 暂无解析
