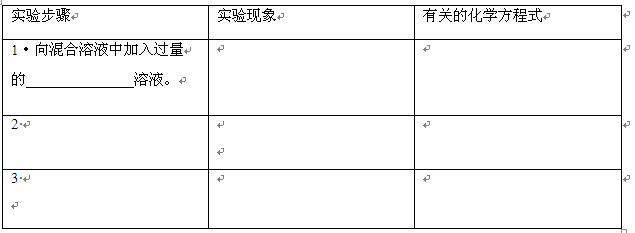
实验室一烧杯中盛有含少量NaCl的CaCl2溶液。请设计实验除去其中的NaCl,以得到纯净的CaCl2溶液。然后根据设计将相关内容填写在下面实验报吉的空格内(有的空格可以不填)
题目
相似考题
更多“实验室一烧杯中盛有含少量NaCl的CaCl2溶液。请设计实验除去其中的NaCl,以得到纯净的CaCl2溶液。然后根据设计将相关内容填写在下面实验报吉的空格内(有的空格可以不填) ”相关问题
-
第1题:
在抗原抗体反应中,通常作为抗原抗体稀释液的溶液是
A.0.70%NaCl溶液
B.0.60%NaCl溶液
C.0.75%NaCl溶液
D.0.85%NaCl溶液
E.0.95%NaCl溶液
正确答案:D
-
第2题:
通过海水晾晒可得粗盐。粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操作流程如下图所示。
根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是( ) 。
(2)操作Ⅰ和操作Ⅱ的名称是( )。该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是( ) (填序号)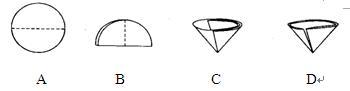
(3)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取( )等措施。
(4)在实验过程中加入过量的NaOH溶液,其实验目的是( ) 。
(5)判断加入的盐酸“适量”的方法是( )。
(6)实验所得精盐的质量_________(填“大于”、“小于”或“等于”)粗盐中NaCl的质量,原因是( )。
答案:解析:(1)水
(2)过滤 D
(3)间歇加热(或“来回移动酒精灯或蒸发皿”)
(4)除尽溶液中的镁离子
(5)滴加盐酸至无气泡放出为止
(6)大于 提纯的过程中有氯化钠生成 -
第3题:
现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2 = CaCO3↓+2NaCl)。反应时CaCl2溶液与沉淀的质量关系如图所示。请解决以下问题: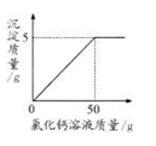
(1)计算样品中NaOH的质量;
(2)计算所加CaCl2溶液的溶质质量分数;
(3)恰好完全反应时烧杯中溶液的pH______7(选填“>”、“<”或“=”)答案:解析:(1)解:设样品中碳酸钠的质量为x,加入的氯化钙溶液中的溶质质量为y
Na2C03+CaCl2=CaC03↓ +2NaCl
106 111 100
x Y 5 g
106/100=x/5g
x=5.3 g
该样品中NaOH的质量为l0 g-5.3 g=4.7 g
(2)111/y=100/5g
y= 5.55 g
所加CaCl2溶液的溶质质量分数=5.55g/50g×l00%=11.1%
答:样品中NaOH的质量为4.7 g,所加CaCl2溶液的溶质质量分数为ll.1%
(3) > -
第4题:
离体蛙心实验中,试分析下列实验因素对蛙心的影响及影响机理 1)0.65Nacl 2ml 2)2%CaCl2 1-2滴 3)1%KCl 1-2滴
正确答案: (1)加0.65%氯化钠,心肌收缩力下降,心率下降,0.65%氯化钠是两栖类动物血浆等渗液,但缺乏钾离子,钙离子等,心肌细胞终末池不发达,贮钙能力差,心肌收缩则更多依赖外源性钙离子,钙离子减少.
(2)加钙离子,心肌收缩力增加,心率增加,钙离子浓度增加,平台期钙离子内流增加,心肌兴奋,收缩耦联增加,心肌收缩力增加;静脉窦自律细胞4期自动去极增加,自律性增加,心率增加
(3)加钾离子,心肌收缩力下降,心率下降,血钾离子增加,细胞内外差距减小,静息电位绝对值减小,减小到-55或-60毫伏,快钠通道失活,兴奋性下降;竞争性抑制钙离子内流,钙离子延缓,心肌兴奋,收缩耦联增加,心肌收缩力增加. -
第5题:
以下溶液用半透膜隔开,渗透方向正确的是()
- A、2mol/L的KCl溶液=2mol/L的蔗糖溶液
- B、0.5mol/L的CaCl2溶液→0.5mol/L的NaCl溶液
- C、0.2mol/L的葡萄糖溶液←0.1mol/L的蔗糖溶液
- D、50g/L的葡萄糖溶液→50g/L的蔗糖溶液
- E、0.5 mol/L的NaCl溶液→0.5 mol/L的葡萄糖溶液
正确答案:C -
第6题:
除去混在Na2CO3粉末中的少量NaHCO3最合理的方法是哪个()。
- A、加热
- B、加NaOH溶液
- C、加盐酸
- D、加CaCl2溶液
正确答案:A -
第7题:
下列选项的括号内是除去杂质所用的试剂,其中错误的是()
- A、苯中有少量杂质苯酚(NaOH溶液)
- B、乙醇中混有少量水(生石灰)
- C、乙酸乙酯中混有少量乙酸(NaOH溶液)
- D、肥皂液中混有少量甘油(Nacl)
- E、以上所用试剂没有错误的
正确答案:C -
第8题:
25℃时CaCO3的溶解度在()最小。()
- A、0.05mol·L-1的AgN03溶液
- B、0.05mol·L-1的CaCl2溶液
- C、0.01mol·L-1的NaCl溶液
- D、纯水
正确答案:B -
第9题:
1升下列四种溶质质量相同的溶液中,渗透压最大的是()。
- A、葡萄糖溶液(M=180)
- B、NaCl溶液(M=58.5)
- C、蔗糖溶液(M=342)
- D、CaCl2溶液(M=111)
正确答案:B -
第10题:
单选题下列溶液中含Cl一浓度最大的是( ).A10mL0.1mol/L的AlCl3溶液
B20mL0.1mol/L的CaCl2溶液
C30mL0.2mol/L的KCl溶液
D100mL0.25mol/L的NaCl溶液
正确答案: A解析:
A项,氯离子的浓度为0.3mol/L;B项,氯离子的浓度为0.4mol/L;C项,氯离子的浓度为0.2mol/L;D项,氯离子的浓度为0.25mol/L. -
第11题:
单选题蒸发温度为-85~55℃时,可以采用()为载冷剂。A氯化钙(CaCl2)水溶液
B氯化钠(NaCl)水溶液
C乙二醇
D乙醇
正确答案: D解析: 暂无解析 -
第12题:
判断题在相同温度下,渗透浓度均为200mmol•L-1的NaCl溶液和CaCl2溶液,其渗透压相等。A对
B错
正确答案: 错解析: 暂无解析 -
第13题:
Ⅱ.(12分)为研究兔红细胞在不同浓度NaCl溶液中的形态变化,请根据以下提供的实验材料与用具,写出实验思路,设计记录实验结果及原因分析的表格,并填入相应内容。
材料与用具:兔红细胞稀释液、质量分数为1.5%的NaCl溶液、蒸馏水、试管、显微镜等。(要求:答题时对NaCl溶液的具体配制、待观察装片的具体制作不作要求)
(1)实验思路:①
正确答案:(1)①配制质量分数由低到1.5%的NaCL溶液,分别等量加入各支试管中。
②向上述各支试管中分别加入等量的兔红细胞稀释液,放置一定时间。
③取兔红细胞稀释液和上述试管中的红细胞稀释液制作装片,用显微镜观察并比较红细胞形态的变化。
-
第14题:
某初中化学教师在一次测验中设计了下列试题.并对部分学生的解题结果进行了统计和分析。
【试题】实验室现有3瓶失去标签的无色溶液。已知它们分别是NaN03、NaCl、Na2C03的溶液,请设计实验方案,将它们一一鉴别。
【考试结果】有30%N学生提交了下面的方案:分别取三种溶液样品少量,放入三支试管中,向三支试管各滴入稀盐酸,有气泡冒出的溶液是Na2C03溶液,再向无明显现象的两支试管里分别滴AgN03溶液,有白色沉淀产生的原溶液是NaCl溶液,无明显现象的原溶液是NaN03溶液。
根据上述信息,回答:
(1)请设计出本实验正确的鉴别方案。
(2)试对上述学生答题错误的原因进行分析。
(3)写出本实验中涉及的有关化学反应方程式。答案:解析:(1)方案为在三种溶液加入过量稀硝酸溶液,产生气泡的原溶液为碳酸钠溶液。在剩余两种溶液中滴加少量硝酸银溶液,产生白色沉淀的原溶液为氯化钠溶液,无现象的原溶液为硝酸钠溶液。 (2)学生的失误在于第一步鉴别碳酸钠溶液时加入盐酸.引入氯离子,从而使剩余两种溶液在滴加硝酸银溶液时均会产生白色溶液.导致剩余两种溶液不能鉴别.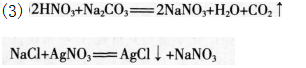
-
第15题:
下列相同的稀溶液,蒸气压最高的是()。
- A、HAC水溶液
- B、CaCl2水溶液
- C、蔗糖水溶液
- D、NaCl水溶液
正确答案:C -
第16题:
在相同温度下,渗透浓度均为200mmol•L-1的NaCl溶液和CaCl2溶液,其渗透压相等。
正确答案:正确 -
第17题:
除去混在NaaCO3粉末中的少量NaHCO3最合理的方法是()。
- A、加热
- B、加NaOH溶液
- C、加盐酸
- D、加CaCl2溶液
正确答案:A -
第18题:
除去混在Na2CO3粉末中的少量NaHCO3最合理的方法是()。
- A、加热
- B、加NaOH溶液
- C、加盐酸
- D、加CaCl2溶液
正确答案:A -
第19题:
中学化学实验中常用到碳酸钠溶液,下列有关叙述错误的是()。
- A、在实验室中,能用碳酸钠溶液制备少量烧碱
- B、实验室制CO2气体时.用饱和碳酸钠溶液除去其中混有的HCl气体
- C、制取乙酸丁酯时,用于除去混有的丁醇和乙酸
- D、做银镜反应实验时,可用热的碳酸钠溶液洗涤掉反应前试管内壁上的油污
正确答案:B -
第20题:
蒸发温度为-85~55℃时,可以采用()为载冷剂。
- A、氯化钙(CaCl2)水溶液
- B、氯化钠(NaCl)水溶液
- C、乙二醇
- D、乙醇
正确答案:C -
第21题:
填空题在中学化学实验中学过的可用于分离或提纯物质的方法很多,请将分离或提纯下列各混合物最适宜的方法的名称填入括号内.(1)除去生石灰中混有的石灰石____.(2)除去碘中混有的碘化钾固体____.(3)除去NaCl晶体中混有的氯化铵____.(4)除去KCl固体中混有的MnO2____.(5)从NaCl溶液中提取NaCl____.正确答案: 加热,升华,加热,过滤,蒸发结晶解析:
(1)加热煅烧石灰石将分解为氧化钙和二氧化碳,从而达到出去杂质的目的;(2)加热使得碘升华为气体,之后在冷却升华,达到提纯的目的;(3)加热晶体使得氯化铵分解为氨气和氯化氢气体,达到提纯的目的;(4)二氧化锰固体难溶于水,将该混合固体加入水中,过滤掉二氧化锰,可达到分离的目的;(5)蒸发结晶氯化钠溶液,可得到纯净的氯化钠. -
第22题:
填空题在中学化学实验中学过的可用于分离或提纯物质的方法很多,请将分离或提纯下列各混合物最适宜的方法的名称填入横线上. (1)除去生石灰中混有的石灰石____. (2)除去碘中混有的碘化钾固体____. (3)除去NaCl晶体中混有的氯化铵____. (4)除去KCl固体中混有的MnO2____. (5)从NaCl溶液中提取NaCl____.正确答案: 加热,升华,加热,过滤,蒸发结晶解析:
(1)加热煅烧石灰石将分解为氧化钙和二氧化碳,从而达到出去杂质的目的;(2)加热使得碘升华为气体,之后在冷却升华,达到提纯的目的;(3)加热晶体使得氯化铵分解为氨气和氯化氢气体,达到提纯的目的;(4)二氧化锰固体难溶于水,将该混合固体加入水中,过滤掉二氧化锰,可达到分离的目的;(5)蒸发结晶氯化钠溶液,可得到纯净的氯化钠. -
第23题:
单选题25℃时CaCO3的溶解度在()最小。A0.05mol·L-1的AgN03溶液
B0.05mol·-1L的CaCl2溶液
C0.01mol·L-1的NaCl溶液
D纯水
正确答案: A解析: 暂无解析
