将0.1 mol/L的氨水(pKb=4.75)和0.1 mol/L的氯化铵溶液等体积混合,再稀释一倍,则溶液的pH是()。A.4.75B.5.75C.9.25D.8.25
题目
将0.1 mol/L的氨水(pKb=4.75)和0.1 mol/L的氯化铵溶液等体积混合,再稀释一倍,则溶液的pH是()。
A.4.75
B.5.75
C.9.25
D.8.25
相似考题
更多“将0.1 mol/L的氨水(pKb=4.75)和0.1 mol/L的氯化铵溶液等体积混合,再稀释一倍,则溶液的pH是()。”相关问题
-
第1题:
将0.1mol·L-1的将0.1mol·L-1的溶液冲稀一倍,下列叙述正确的是( )。A、HOAc的解离度增大
B、溶液中有关离子浓度增大
C、HOAc的解离常数增大
D、溶液的pH值降低答案:A解析:HOAc即乙酸。A项,解离度是指电解质达到解离平衡时,已解离的分子数和原有分子数之比,习惯上用百分率来表示。溶液稀释,解离度增大。BC两项,在酸碱平衡过程中,习惯用弱电解质的解离常数来描述弱电解质的解离,计算浓度和解离能力,与物质的浓度无关。D项,溶液稀释一倍,酸性溶液的pH值增大。 -
第2题:
等体积混合0.1 mol/L盐酸和0.06 mol/L氢氧化钡溶液,混合后溶液的pH=____________.答案:解析:12【解题指要】
(1)设酸和碱溶液的体积均为1 L,则盐酸溶液中含HCl为0.1 mol/L×1 L=0.1 mol;
Ba(OH)2溶液中含Ba(OH)2为0.06 mol/L×l L=0.06 mol.
(2)两溶液混合时,要发生化学反应
因此,混合后可能有以下三种情况:
①恰好完全反应.因BaCl2是强酸强碱盐,所以溶液显中性.
②酸有剩余,溶液显酸性.
③碱有剩余,溶液显碱性.
究竟属于哪一种情况,需经计算才能知道.
设与盐酸完全反应需Ba(OH)2xmol,则
所以Ba(OH)2剩余:0.06 mol-0.05 mol=0.01mol.
(3)计算混合后溶液的pH.

OH一的物质的量浓度为0.005 mol/L×2=0.01mol/L,则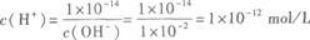
即pH=12. -
第3题:
将0.1mol/L的NaOH溶液与0.2mol/L的HAC溶液等体积混合,混合溶液具有缓冲作用。
正确答案:正确 -
第4题:
将0.1mol/L的HAc与0.1mol/L的NaAc混合溶液中加水稀释至原的体积的2倍,其H+浓度和pH值变化为()。
- A、原来的1/2倍和增大
- B、原来的1/2倍和减小
- C、减小和增大
- D、不变和不变
正确答案:D -
第5题:
下列溶液中,不具有缓冲作用的是()
- A、纯水。
- B、0.1mol/LHAc溶液和0.1mol/LNaAc溶液的等体积混合溶液。
- C、新鲜血浆。
- D、0.1mol/1HAc溶液和0.05mol/LNaOH溶液的等体积混合溶液。
正确答案:A -
第6题:
0.1mol/l的HCl溶液和0.1mol/l的HAc(Ka=1.8×10-5),溶液等体积混合后,pH值为()。
- A、1.0
- B、2.0
- C、1.3
- D、1.5
正确答案:C -
第7题:
以下溶液稀释10倍时,pH值改变最大的是()
- A、0.1mol·L-1NH4Ac
- B、0.1mol·L-1NaAc
- C、0.1mol·L-1HAc
- D、0.1mol·L-1HCl
正确答案:D -
第8题:
0.1mol·L-1NaOH和0.1mol·L-1NH3H2O等体积混合,溶液中总的[OH-] /(mol·L-1为()。
- A、0.1013
- B、0.1
- C、0.05
- D、0.052
正确答案:C -
第9题:
问答题氨性缓冲溶液中,氨的浓度为0.5mol∕L,氯化铵的浓度为1.0mol∕L,氨的pKb=4.75,其pH是多少?正确答案: pH=14.00-pKb+lg[(氨)∕(氯化铵)]
=14.00-4.75+lg(0.5∕1.0)
=8.95
该氨性缓冲溶液的pH=8.95。解析: 暂无解析 -
第10题:
单选题40mL0.1mol/L KNO3溶液和60mL0.2mol/L K2SO4溶液混合,若混合时溶液体积的微小变化忽略不计,则混合溶液中K+的物质的量浓度为( ).A0.3mol/L
B0.24mol/L
C0.28mol/L
D0.16mol/L
正确答案: D解析:
混合后溶液中钾离子的物质的量为0.04×0.1+0.06×0.2×2=0.028mol,因此,混合溶液中钾离子的物质的量浓度为0.28mol/L. -
第11题:
单选题向一定体积的0.1mol/L的醋酸溶液中加入等体积的蒸馏水后,则下列叙述正确的是()A溶液的pH值变小
B醋酸的电离度增大
C溶液的导电能力减弱
D中和此溶液所需的0.1mol/LNaOH溶液的体积增加
正确答案: B解析: 暂无解析 -
第12题:
单选题下列各组溶液中,具有缓冲溶液性质的是()。A0.1mol·L-1NaOH溶液与0.2mol·L-1HAc等体积混合
B0.1mol·L-1NaAc溶液与0.2mol·L-1HCI等体积混合
C0.1mol·L-1NH3·H2O与0.1mol·L-1HCl等体积混合
D0.1mol·L-1HAc与0.1mol·L-1NaOH等体积混合
正确答案: B解析: 暂无解析 -
第13题:
将6 mL 0.2 mol/L盐酸与10 mL 0.1 mol/L氨水混合,完全反应后,溶液中各种离子浓度的相对大小是.答案:解析: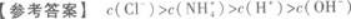 【解题指要】(1)首先要强调,将两种溶液混合时必须考虑这一过程中是否发生化学反应.如本题是将盐酸与氨水混合,会发生化学反应:
【解题指要】(1)首先要强调,将两种溶液混合时必须考虑这一过程中是否发生化学反应.如本题是将盐酸与氨水混合,会发生化学反应:

根据HCl和NH3的数量的不同.可能有三种情况:
①恰好完全反应,此时就变成NH4Cl溶液;
②HCl有剩余,此时就是NH4Cl和HCl的混合溶液;
③NH3有剩余,此时就是NH4Cl与NH3的混合溶液.
(2)盐酸中HCl的物质的量为:0.2 mol/L×0.006 L=0.001 2 mol.
氨水中NH3的物质的量为:0.1 mol/L×0.01 L=0.001 mol.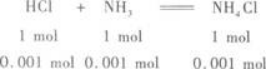
所以,反应后生成NH4Cl 0.001 mol,剩余的HCl为0.001 2 mol-0.001 mol=0.000 2 mol.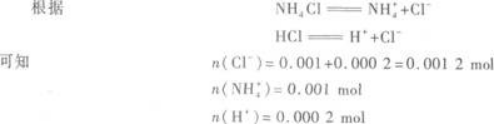
以上物质的量的大小顺序就是离子浓度的大小顺序.
另外,一般情况下,溶液均指水溶液,所以溶液中还有水电离出来的H+和OH-两种离子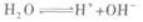
此题中酸有剩余,所以c(H+)一定大于c(OH-).
-
第14题:
已知 Ksp [Mg(OH)2] =5×10-12,现将等体积的 0.1mol/L。Mg+2溶液和 0.1mol/L NaOH溶液混合,则( )。
A.有沉淀析出 B.形成饱和溶液 C.溶液未饱和 D.无法判断答案:A解析:
-
第15题:
下列溶液中具有缓冲溶液性质的是哪一种()?
- A、0.1mol/LNaAc溶液与0.2mol/LHCl溶液等体积混合
- B、0.1mol/LNH3·H2O溶液与0.1mol/LHCl溶液等体积混合
- C、0.1mol/LNaOH溶液与0.2mol/LHAc溶液等体积混合
- D、0.1mol/LHAc溶液与0.1mol/LNaOH溶液等体积混合
正确答案:C -
第16题:
40 mL 0.1 mol·L–1HAc与20 mL 0.1 mol·L–1NaOH混合后,溶液的pH值为()
- A、3.1
- B、9.25
- C、4.75
- D、5.3
正确答案:C -
第17题:
以下各组溶液中,哪组不是缓冲溶液()。
- A、0.2mol·L-1NH4Cl与0.1mol·L-1NaOH等体积混合
- B、0.1mol·L-1NaOH与0.1mol·L-1HAc等体积混合
- C、0.1mol·L-1NaOH与0.2mol·L-1HAc等体积混合
- D、0.1mol·L-1NaOH与0.2mol·L-1Na2HPO4等体积混合
正确答案:B -
第18题:
0.1mol/L的HAC溶液与0.1mol/L的NaOH溶液等体积混合后,该溶液的PH是()。
- A、5.28
- B、7.00
- C、8.72
- D、10
正确答案:C -
第19题:
氨性缓冲溶液中,氨的浓度为0.5mol∕L,氯化铵的浓度为1.0mol∕L,氨的pKb=4.75,其pH是多少?
正确答案: pH=14.00-pKb+lg[(氨)∕(氯化铵)]
=14.00-4.75+lg(0.5∕1.0)
=8.95
该氨性缓冲溶液的pH=8.95。 -
第20题:
下列各组溶液中,具有缓冲溶液性质的是()。
- A、0.1mol·L-1NaOH溶液与0.2mol·L-1HAc等体积混合
- B、0.1mol·L-1NaAc溶液与0.2mol·L-1HCI等体积混合
- C、0.1mol·L-1NH3·H2O与0.1mol·L-1HCl等体积混合
- D、0.1mol·L-1HAc与0.1mol·L-1NaOH等体积混合
正确答案:A -
第21题:
单选题下列溶液用酸碱滴定法能准确滴定的是()。A0.1mol∙L-1HF(pKa=3.18)
B0.1mol∙L-1HCN(pKa=9.21)
C0.1mol∙L-1NaAc[pKa(HAc)=4.74]
D0.1mol∙L-1NH4Cl[pKb(NH3)=4.75]
正确答案: C解析: 暂无解析 -
第22题:
单选题下列溶液中具有缓冲溶液性质的是哪一种()?A0.1mol/LNaAc溶液与0.2mol/LHCl溶液等体积混合
B0.1mol/LNH3·H2O溶液与0.1mol/LHCl溶液等体积混合
C0.1mol/LNaOH溶液与0.2mol/LHAc溶液等体积混合
D0.1mol/LHAc溶液与0.1mol/LNaOH溶液等体积混合
正确答案: B解析: 必须是弱酸与弱酸盐或弱碱与弱碱盐组成的溶液才是缓冲溶液。 -
第23题:
单选题将0.1mol/L的HAc与0.1mol/L的NaAc混合溶液中加水稀释至原的体积的2倍,其H+浓度和pH值变化为()。A原来的1/2倍和增大
B原来的1/2倍和减小
C减小和增大
D不变和不变
正确答案: B解析: 暂无解析 -
第24题:
单选题以下溶液稀释10倍时pH改变最小的是()A0.1mol·L-1NH4OAc溶液
B0.1mol·L-1NaOAc溶液
C0.1mol·L-1HOAc溶液
D0.1mol·L-1HCl溶液
正确答案: D解析: 暂无解析
