在标准状态下,若氧气(视为刚性双原子分子)和氦气的体积之比V1/V2=1/2,则其内能之比E1/E2为( )。A.3/10 B.1/2 C.5/6 D.5/3
题目
B.1/2
C.5/6
D.5/3
相似考题
更多“在标准状态下,若氧气(视为刚性双原子分子)和氦气的体积之比V1/V2=1/2,则其内能之比E1/E2为( )。”相关问题
-
第1题:
在标准状态下,当氢气和氦气的压强与体积都相等时,氢气和氦气的内能之比为( )。A、 5/3
B、 3/5
C、 1/2
D、 3/2答案:A解析:
-
第2题:
在标准状态下,若氢气(可视作刚性双原子分子的理想气体)和氦气的体积比为V1/V2=1/2,则其内能之比E1/E2为( )。A.3/10
B.2/3
C.5/6
D.5/3答案:C解析:
-
第3题:
—定量的理想气体,经过等体过程,温度增量△T,内能变化△E1,吸收热量Q1;若经过等压过程,温度增量也为△T,内能变化△E2,吸收热量Q2,则一定是:A.△E2=△E1,Q2>Q1
B.△E2=△E1,Q21
C.△E2>△E1,Q2>Q1
D.△E21,Q21答案:A解析: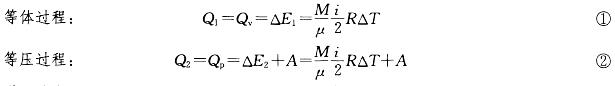
对于给定的理想气体,内能的增量只与系统的起始和终了状态有关,与系统所经历的过程
无关,△E1=△E2。
比较式①和式②,注意到A>0,显然Q2>Q1。 -
第4题:
V1、V2、V3分别是土在天然状态下、开挖后松散状态下和经回填压实后的体积,则土的最初可松性系数是()
- A、V1/V2
- B、V2/V1
- C、V1/V3
- D、V3/V1
正确答案:A -
第5题:
标准状态下,若氧气和氦气的体积比V1/V2=1/2,则其内能E1/E2为()
- A、1/2
- B、5/6
- C、3/2
- D、1/3
正确答案:B -
第6题:
1mol氧气和2mol氮气组成混合气体,在标准状态下,氧分子的平均能量为(),氮分子的平均能量为();氧气与氮气的内能之比为()。
正确答案:9.42×10-21;9.42×10-21;1:2 -
第7题:
在相同的温度和压强下,单位体积的氦气与氢气(均视为刚性分子理想气体)的内能之比为:()
- A、1
- B、2
- C、3/5
- D、5/6
正确答案:C -
第8题:
在标准状态下,若氧气(视为刚性双原子分子)和氦气的体积之比V1/V2=1/2,则其内能之比E1/E2为()。
- A、3/10
- B、1/2
- C、5/6
- D、5/3
正确答案:C -
第9题:
单选题在标准状态下,若氧气(视为刚性双原子分子)和氦气的体积之比V1/V2=1/2,则其内能之比E1/E2为()。A3/10
B1/2
C5/6
D5/3
正确答案: C解析: 暂无解析 -
第10题:
单选题一定量的理想气体,经过等体过程,温度增量△T,内能变化△E1,吸收热量Q1;若经过等压过程,温度增量也为△T,内能变化△E2,吸收热量Q2,则一定是:()A△E2=△E1,Q2>Q1
B△E2=△E1,Q21
C△E2>△E1,Q2>Q1
D△E2<△E1,Q21
正确答案: C解析: 暂无解析 -
第11题:
单选题在相同的温度和压强下,单位体积的氦气与氢气(均视为刚性分子理想气体)的内能之比为:()A1
B2
C3/5
D5/6
正确答案: C解析: 暂无解析 -
第12题:
单选题在标准状态下,体积比为1:2的氧气和氦气(均视为刚性分子理想气体)相混合,混合气体中氧气和氦气的内能之比为:()A1:2
B5:3
C5:6
D10:3
正确答案: C解析: E=(1/2)i(m/M)RT=(1/2)ipV。 -
第13题:
在相同的温度和压强下,单位体积的氦气与氢气(均视为刚性分子理想气体)的内能之比为:A. 1
B. 2
C. 3/5
D. 5/6答案:C解析:提示:E=(1/2)ipV。 -
第14题:
在标准状态下,若氧气(视为刚性双原子分子)和氦气的体积之比V1/V2=1/2,则其内能之比E1/E2为( )。A.3/10
B.1/2
C.5/6
D.5/3答案:C解析:
-
第15题:
在标准状态下,体积比为1:2的氧气和氦气(均视为刚性分子理想气体)相混合,混合气体中氧气和氦气的内能之比为:()
- A、1:2
- B、5:3
- C、5:6
- D、10:3
正确答案:C -
第16题:
已知突扩前后管段的管径之比d1/d2=0.5,则突扩前后断面平均流速之比v1/v2=()。
- A、4
- B、2
- C、1
- D、0.5
正确答案:A -
第17题:
在标准状态下,氧气和氦气体积比为V1/V2=1/2,都视为刚性分子理想气体,则其内能之比E1/E2为:()
- A、3/10
- B、1/2
- C、5/6
- D、5/3
正确答案:C -
第18题:
一定量的理想气体,经过等体过程,温度增量△T,内能变化△E1,吸收热量Q1;若经过等压过程,温度增量也为△T,内能变化△E2,吸收热量Q2,则一定是:()
- A、△E2=△E1,Q2>Q1
- B、△E2=△E1,Q21
- C、△E2>△E1,Q2>Q1
- D、△E2<△E1,Q21
正确答案:A -
第19题:
两个体积相同的容器中,分别贮有氮气和氢气,若它们的压强相同,以E1和E2分别表示氮气和氢气的内能,则()。
- A、E1=E2
- B、E1=>E2
- C、E1=<E2
- D、无法确定
正确答案:C -
第20题:
已知HCl溶液的浓度为H3PO4溶液浓度的2倍,如以酚酞为指示剂,用同一NaOH标准溶液滴定同体积的HCl和H3PO4溶液,消耗的NaOH标准溶液的体积分别为 V1和V2,则V1和V2的关系为()。
- A、V1=V2
- B、V1=2V2
- C、V2=2V1
- D、V1=4V2
正确答案:A -
第21题:
单选题已知突然扩大管道的管径之比d1/d2=0.5,则其相应的水流流速之比v1/v2=()。A1
B2
C3
D4
正确答案: D解析: 暂无解析 -
第22题:
单选题设G1=(V1,E1)和G2=(V2,E2)为两个图,如果V1V2,E1E2则称()。AG1是G2的子图
BG2是G1的子图
CG1是G2的连通分量
DG2是G1的连通分量
正确答案: A解析: 暂无解析 -
第23题:
单选题一定量的理想气体经过等体过程,温度增量ΔT,内能变化ΔE1,吸收热量Q1;若经过等压过程,温度增量也为ΔT,内能变化ΔE2,吸收热量Q2,则一定是( )。[2012年真题]AΔE2=ΔE1,Q2>Q1
BΔE2=ΔE1,Q2<Q1
CΔE2>ΔE1,Q2>Q1
DΔE2<ΔE1,Q2<Q1
正确答案: A解析:
两过程温度增量均为ΔT,又内能增量ΔE=(m/M)·(i/2)·RΔT,则ΔE2=ΔE1。对于等体过程,Q1=ΔE1+W1,等体过程不做功,W1=0,Q1=ΔE1=(m/M)·(i/2)·RΔT。对于等压过程,Q2=ΔE2+W2=(m/M)·(i/2+1)·RΔT。所以Q2>Q1。 -
第24题:
单选题在标准状态下,当氢气和氦气的压强与体积都相等时,氢气和氦气的内能之比为( )。[2014年真题]A5/3
B3/5
C1/2
D3/2
正确答案: D解析:
分子内能方程为:E内=(m/M)·(iRT/2)=ipV/2。注意到氢为双原子分子,氦为单原子分子,即i(H2)=5,i(He)=3;又p(H2)=p(He),V(H2)=V(He),故E内(H2)/E内(He)=i(H2)/i(He)=5/3。
