某第4周期的元素,当该元素原子失去一个电子成为正1价离子时,该离子的价层电子排布式为3d10则该元素的原子序数是: A. 19 B. 24 C.29 D. 36
题目
B. 24
C.29
D. 36
相似考题
更多“某第4周期的元素,当该元素原子失去一个电子成为正1价离子时,该离子的价层电子排布式为3d10则该元素的原子序数是: ”相关问题
-
第1题:
某元素原子的核外电子排布为1S22S22P63S1,该元素的原子序数为(),核内质子数为(),元素符号为()。参考答案: ll;l1;Na
-
第2题:
某元素最高氧化数为+6,最外层电子数为1,原子半径是同族元素中最小的。下列叙述中不正确的是( )。A.外层电子排布为3d54s1
B.该元素为第四周期、ⅥB族元素铬
C.+3价离子的外层电子排布式为3d24s1
D.该元素的最高价氧化物的水合物为强酸答案:C解析:根据题意,最高氧化数为+6的元素有VIA族和VIB族元素;而已知最外层只有一个电子,故只能是VIB族元素;在由已知中最后一个条件“原子半径是同族元素中最小的”,可确定该元素是VIB组中的Cr,Cr的电子排布式为
,可得出以下结论:
外层电子排布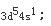
因为周期数等于电子层数,等于最高主量子数,即第四周期。他的最后一个电子填充在d亚层上,所以它是副族元素,其族数等于[(n-1)d+ns]电子层上的电子数,对Cr来讲为5+1=6,即ⅥB族元素;
因为原子失去电子时,首先失去最外层上的电子,继而再失去次外层上的d电子。所以+3价离子的外层电子排布为
Cr的最高价氧化物CrO3,其水合物为H2CrO4或H2Cr2O7均为强酸。 -
第3题:
当n=4时,该电子层电子的最大容量为()个;某元素原子在n=4的电子层上只有2个电子,在次外层l=2的轨道中有10个电子,该元素符号是(),位于周期表中第四周期,第()族,其核外电子排布式为()。
正确答案: 32;Zn;ⅡB;1s22s22p63s23p63d104s2 -
第4题:
元素的性质随着原子序数的递增呈现周期性变化的原因是()。
- A、元素原子的核外电子排布呈周期性变化
- B、元素原子的电子层数呈现周期性变化
- C、元素化合价呈周期性变化
- D、元素原子半径呈周期性变化
正确答案:A -
第5题:
若某基态原子的外围电子排布为4d15s2,则下列说法正确的是()
- A、该元素基态原子中共有3个电子
- B、该元素原子核外有5个电子层
- C、该元素原子最外层共有3个电子
- D、该元素原子M能层共有8个电子
正确答案:B -
第6题:
某元素原子主量子数n为4的电子层上有7个电子,该元素原子外层电子构型是(),未成对电子数为(),原子核外电子分布式为(),该元素原子序数是(),它位于第()周期,第()族,最高氧化数()。
正确答案:4s24p5;1;1s22s22p63s23p63d104s24p5;35;四;ⅦA;+7 -
第7题:
已知某元素+3价离子的电子排布式为1s22s22p63s23p63d5,则该元素在周期表中哪一周期、哪一族?()
- A、四,Ⅷ
- B、五,VB
- C、三,VA
- D、六,ⅢB
正确答案:A -
第8题:
某元素为第四周期元素、易失去2个电子形成+2价阳离子,则n=3电子层处于全充满状态,该元素为()。
- A、Cd
- B、Sc
- C、CU
- D、Zn
正确答案:D -
第9题:
第三电子层有10个电子的某元素,其原子序数是(),该元素属第()周期、()族。
正确答案:22;四;ⅣB -
第10题:
已知某元素为第四周期元素,其二价离子的外层有18个电子,则该元素的原子序数为(),元素符号为(),在周期表中的()区,第()族。
正确答案:20;Ca;S;ⅡA -
第11题:
单选题某第4周期的元素,当该元素原子失去一个电子成为正1价离子时,该离子的价层电子排布式为3d10,则该元素的原子序数是:()A19
B24
C29
D36
正确答案: B解析: 暂无解析 -
第12题:
单选题某第4周期的元素,当该元素原子失去一个电子成为正1价离子时,该离子的价层电子排布式为3d10,则该元素的原子序数是( )。[2011年真题]A19
B24
C29
D36
正确答案: D解析:
元素原子失去一个电子成为正1价离子时,该离子的价层电子排布式为3d10,说明其原子的外层电子排布式为:3d104s1,故为第四周期IB的29号Cu。 -
第13题:
某元素原子的核外电子排布为1S22S22P63S1,该元素的原子序数为l1,核内质子数为11 ,元素符号为( )
正确答案:Na
-
第14题:
已知某元素+2价离子的核外电子排布式为:[Ar]3d5,该元素在周期表中处于()周期、()族、()区,元素符号是()。
正确答案:第四;ⅦB;d;Mn -
第15题:
某元素的基态价层电子构型为5d66s2,请给出比该元素的原子序数小4的元素的基态原子电子组态。
正确答案: 按构造原理,该元素的基态电子组态为[Xe]4f145d24s2。 -
第16题:
某元素的金属性强,一般是指()。
- A、该元素的原子失去电子而成为阳离子的趋势强
- B、该元素有较大的硬度
- C、该元素有金属光泽
- D、该元素的最外层电子数多于4个
正确答案:A -
第17题:
某元素的二价阳离子核外有24个电子,该元素原子的外层电子构型是()。
正确答案:3d64S2 -
第18题:
已知某元素+3价离子的核外电子排布式为1s22s22p63s23p63d5,该元素在周期表中属于()
- A、ⅤB族
- B、ⅢB族
- C、Ⅷ族
- D、ⅤA族
正确答案:C -
第19题:
某第4周期元素,当该元素原子失去一个电子成为正1价离子时,该离子的价层电子排布式为3d10,则该元素的原子序数为()。
- A、19
- B、24
- C、29
- D、36
正确答案:C -
第20题:
某一元素的原子序数为24,试问: (1)核外电子总数是多少? (2)它的电子排布式? (3)价电子层结构; (4)元素所处的周期、族、区?
正确答案: (1)核外电子总数是24
(2)它的电子排布式:1s22s22p63s23p63d54s1
(3)价电子层结构:3d54s1
(4)元素所处的四周期、ⅥB族、d区 -
第21题:
Fe元素的原子序数为26,其电子排布式为(),该元素属于第周期()族。配离子[Fe(CN)6]4-中Fe2+的杂化类型为(),配离子空间构型为()。
正确答案:[Ar]3d64s2;四;Ⅷ;d2sp3;正八面体 -
第22题:
某元素的最高正价为+6,最外层电子数为1,原子半径是同族中最小的,试写出该元素的电子结构式、名称及元素符号。
正确答案: 该元素的电子结构式[Ar]3d54s1、名称铬及元素符号Cr。 -
第23题:
单选题某元素最高氧化数为+6,最外层电子数为1,原子半径是同族元素中最小的。下列叙述中哪一个不正确()?A外层电子排布为3d54s1
B该元素为第四周期、VIB族元素铬
C+3价离子的外层电子排布式为3d24s1
D该元素的最高价氧化物的水合物为强酸
正确答案: C解析: 暂无解析
