标准状况下,铁与盐酸发生反应产生44.8升氢气,如果盐酸过量,则参加反应的铁为()g。A28B56C112D224
题目
标准状况下,铁与盐酸发生反应产生44.8升氢气,如果盐酸过量,则参加反应的铁为()g。
A28
B56
C112
D224
相似考题
更多“标准状况下,铁与盐酸发生反应产生44.8升氢气,如果盐酸过量,则参加反应的铁为()g。 ”相关问题
-
第1题:
将8.4 g铁粉跟50 mL盐酸充分混合反应后,有固体剩余,同时收集到1.12 L(标准状况下)H2.原盐酸的物质的量浓度为____________mol/L.答案:解析:2 【解题指要】
(1)铁粉与盐酸混合固体有剩余,即铁粉过量.所以根据反应生成H2的体积,可求得盐酸
中HCl的物质的量.
设50 mL盐酸中HCl的物质的量为xmol,则
所以盐酸的物质的量浓度为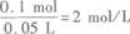

题目已经给出V=0.05 L,所以,只要求得溶质(HCl)的物质的量n代入上式,即可求得c.在
用上式时,应注意V的单位应是“L”,不能用“mL”代入.
(3)Fe与HCl反应的生成物是FeCl2,不是FeCl3.注意不要写错,否则不能得到正确答案. -
第2题:
高铁酸盐在能源、环境保护等方面有着广泛的用途,可以用电解法制高铁酸盐(已知高铁酸盐在酸性条件下不稳定),总反应式为 下列说法正确的是()。A.铁为阳极.发生还原反应
下列说法正确的是()。A.铁为阳极.发生还原反应
B.铁为阴极,浓NaOH为电解液
C.阴极发生的电极反应为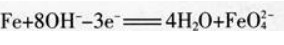
D.标准状况下,铁失去3 mol电子可以在阴极得到33.6 L氢气答案:D解析:由总反应知,铁为阳极,发生氧化反应,电解质溶液应为浓NaOH溶液,A、B两项错误;Fe在反应中失去6个电子,C项错误;根据总反应式可知,铁失去3mol电子在阴极得到1.5 molH2,标准状况下H2体积为33.6 L,D项正确。 -
第3题:
3、某金属能与盐酸反应产生氢气,该金属与锌组成的原电池中,锌为负极,则该金属可能是()
A.铝
B.铜
C.铁
D.镁
Pt -
第4题:
.6g Na2CO3·10H2O与质量分数为36.5%(密度1.19g/cm3)的盐酸完全反应,消耗这种盐酸溶液多少毫升?在标准状况下,反应答案:解析:
-
第5题:
一、考题回顾

二、考题解析
【教学过程】
环节一:生活导入
【提出问题】厨房用来盛装醋的容器,一般不采用铝制品,原因是什么?
【学生回答】铝制品会与醋酸发生化学反应。
【教师引导】金属与其他酸能否发生反应?
环节二:新课教学
【教师演示实验】镁条与盐酸的反应,检验生成的气体。
【提出问题】镁条与盐酸反应生成的气体是何种气体?
【学生回答】试管口接近酒精灯火焰,能听到清脆的爆鸣声,判断生成的气体是氢气。
【提出问题】铁、锌、铜能否与盐酸发生反应生成氢气,这四种金属与硫酸反应的实验现象是怎样的,反应的化学方程式应该如何书写。
(学生自主实验环节,分别进行镁、锌、铁、铜与盐酸、硫酸的反应,记录发生反应的实验现象,反应的剧烈程度,书写反应的方程式。)
【学生回答,教师总结】
镁、锌、铁都能与盐酸、硫酸反应生成氢气,铜不能与盐酸、硫酸发生反应,书写化学方程式如下:
【提出问题】以小组为单位思考如下的问题:
①哪些金属能与盐酸、稀硫酸发生反应?反应的剧烈程度如何?反应后生成了什么气体?哪些金属不能与盐酸、稀硫酸发生反应?根据反应时是否有氢气产生,将金属分为两类。
②对于能发生的反应,从反应物和生成物的物质类别如单质、化合物的角度分析,这些反应有什么特点?将这一类反应与化合反应、分解反应进行比较。
【学生回答,教师总结】
①镁、锌、铁能与酸发生反应,反应剧烈程度由大到小依次为镁、锌、铁、铜,且镁、铁、锌与酸反应均放出氢气,铜不与酸反应;
②这些反应都属于一种单质和一种化合物反应生成另外一种单质和另外一种化合物的反应。反应类型不同于化合反应、分解反应。
【教师引导】这几个反应都是由一种单质与一种化合物的反应,生成另一种单质和另一种化合物。这种反应叫做置换反应。
【提出问题】通过金属与酸反应实验的探究,你能够得到什么结论?
【学生回答】镁、锌、铁的金属活泼性比铜强,他们能置换出酸中的氢,而反应速度镁大于锌,锌大于铁,所活动性镁大于锌大于铁。
环节三:巩固提高
下列反应属于化合反应、分解反应、置换反应中那种反应类型?。 答案:解析:
答案:解析:
