已知,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是: A.Zn、Fe2+和Cu B.Fe2+和Cu C. Zn、Fe2+和H2 D.Zn和Fe2+
题目
 ,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是:
,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是:
A.Zn、Fe2+和Cu B.Fe2+和Cu
C. Zn、Fe2+和H2 D.Zn和Fe2+
相似考题
参考答案和解析
 高的电对中的氧化态反应。
高的电对中的氧化态反应。更多“已知,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是: ”相关问题
-
第1题:
已知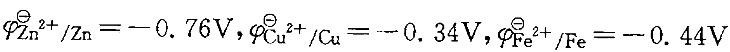 ,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是:
A.Zn、Fe2+和Cu
,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是:
A.Zn、Fe2+和Cu
B.Fe2+和Cu
C. Zn、Fe2+和H2
D.Zn和Fe2+答案:B解析:提示:加入铁钉是还原态,它能和电极电势比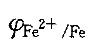 高的电对中的氧化态反应。
高的电对中的氧化态反应。 -
第2题:
有一混合酸溶液,其中HF的浓度为1.0mol/L,HAc的浓度为0.10mol/L,求溶液中H+,F-,Ac-,HF和HAc的浓度已知:Ka(HF)=3.53×10-4 Ka(HAc)=1.76×10-5
正确答案: [H+]=0.0188(M)
[F-]=0.0188(M)
[Ac-]=9.36×10-5(M)
[HF]=0.98(M)
[HAc]=0.1(M) -
第3题:
将铜片插入盛有0.5mol/L的CuSO4溶液的烧杯中,银片插入盛有0.5mol/L的AgNO3,溶液的烧杯中,已知:φθ(Ag+/Ag)=0.7996V, φθ(Cu2+/Cu)=0.337V写出该原电池的符号
正确答案:(-)Cu│Cu2+(0.5M)‖Ag+(0.5M)│Ag(+) -
第4题:
粗纤维测定前去除碳酸盐用的试剂是()
- A、0.5mol/L盐酸溶液
- B、1.0mol/L盐酸溶液
- C、0.5mol/L硝酸溶液
- D、1.0mol/L硝酸溶液
正确答案:A -
第5题:
在30ml 1mol/L氯化钠溶液和40ml 1mol/L氯化钙溶液混合后,混合溶液中氯离子摩尔浓度为()。
- A、0.5mol/L
- B、1.0mol/L
- C、0.67mol/L
- D、2.0mol/L
正确答案:B -
第6题:
静态法钠度测定时,最好使用内充()KCL溶液的甘汞电极。
- A、0、1mol/L;
- B、3、3mol/L;
- C、1、0mol/L;
- D、饱和。
正确答案:A -
第7题:
将铜片插入盛有0.5mol/L的CuSO4溶液的烧杯中,银片插入盛有0.5mol/L的AgNO3,溶液的烧杯中,已知:φθ(Ag+/Ag)=0.7996V, φθ(Cu2+/Cu)=0.337V写出电极反应式和原电池的电池反应
正确答案:电极反应式: (-) Cu2++ 2e-←→ Cu (+) Ag++ e-←→ Ag
电池反应式: Cu+2Ag+←→ 2Ag+Cu2+ -
第8题:
在下列原电池中:(-)Zn│ZnSO4(1.0mol/L)‖C、uSO4(1.0mol/L)│C、u(+),如果降低Zn2+的浓 度,其电动势将()。
- A、增大
- B、减小
- C、不变
- D、无法判断
正确答案:A -
第9题:
CaCO3能溶于HAc溶液中。若沉淀达到溶解平衡时溶液中的[HAc]为1.0mol·L-1,且室温下反应产物H2CO3在水溶液中的饱和浓度为0.040mol·L-1,求1.0L溶液中能溶解()CaCO3。
正确答案:2.3 -
第10题:
单选题除去ZnSO4溶液所含少量CuSO4最好选用下列试剂中的( )。ANH3水
BNaOH
CZn粉
DH2S
正确答案: B解析:
向溶液中加锌粉,发生置换反应如下:
Zn+CuSO4→ZnSO4+Cu -
第11题:
单选题将7.8gNaO和2.7gAl同时放入一定量的水中,充分反应后得到100mL溶液,再向该溶液中缓慢通入HCl气体3.36L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是()。A反应过程中得到3.36L(标准状况)的气体
B反应结束得到3.9g的沉淀
C反应结束得到的溶液中c(Na+)=c(Cl-)+c(OH-)
D反应结束得到的溶液中c(NaCl)=1.0mol·L-1
正确答案: D解析: 暂无解析 -
第12题:
问答题1.0mol/L的NaCl溶液500mL中含有NaCl多少克?已知NaCl的摩尔质量为58.5g/mol正确答案: 根据m=nM,n=cV得
m=c•V•M=1.0×0.5×58.5=29.5(g)
含29.25gNaCl。解析: 暂无解析 -
第13题:
邻硝基苯酚在
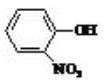 在1.0mol/L溶液与0.5mol/L溶液中OH伸缩振动频率发生什么变化?为什么?
在1.0mol/L溶液与0.5mol/L溶液中OH伸缩振动频率发生什么变化?为什么?
不变化;邻硝基苯酚在上述两个浓度溶液中都生成了分子内氢键,分子内氢键不受溶液浓度的影响。
略 -
第14题:
1.0mol/L的NaCl溶液500mL中含有NaCl多少克?已知NaCl的摩尔质量为58.5g/mol
正确答案: 根据m=nM,n=cV得
m=c•V•M=1.0×0.5×58.5=29.5(g)
含29.25gNaCl。 -
第15题:
将铜片插入盛有0.5mol/L的CuSO4溶液的烧杯中,银片插入盛有0.5mol/L的AgNO3,溶液的烧杯中,已知:φθ(Ag+/Ag)=0.7996V, φθ(Cu2+/Cu)=0.337V 求该电池的电动势
正确答案: E = E°- (0.0592/2)Lg([Cu2+]/[Ag+]2) -
第16题:
0.1mol/l一元弱酸HA和1.0mol/l一元弱酸HB等体积混合,混合后溶液中的氢离子浓度应为()(HAKa=1.0×10-5,HBKa=1.0×10-6)。
- A、2.8×10-3mol/l
- B、2.0×10-3mol/l
- C、1.0×10-3mol/l
- D、1.4×10-4mol/l
- E、1.4×10-3mol/l
正确答案:E -
第17题:
向Al2(SO4)3和CuSO4的混合溶液中放入一个铁钉,其变化是()。
- A、生成A1、H2和Fe2+
- B、生成A1、Cu和Fe2+
- C、生成Cu和Fe2+
- D、生成Cu
正确答案:C -
第18题:
在0.10mol·L-1[Ag(NH3)2]+溶液中,含有1.0mol·L-1游离氨,溶液中Ag+的浓度为()。
正确答案:8.9×10-9mol·L-1 -
第19题:
除去ZnSO4溶液中所含的少量CuSO4,最好选用下列物种中的()
- A、NH3·H2O
- B、NaOH
- C、Zn
- D、H2S
正确答案:C -
第20题:
将等体积的0.80mol·L-1HCl、0.50mol·L-1KOH和0.60mol·L-1KOH溶液相混合,在得到的溶液中各溶质的物质的量浓度是()。
正确答案:0.10mol·L-1 -
第21题:
欲将蛋白质从水中析出而又不变性,应加入()。
- A、饱和Na2SO4溶液
- B、福尔马林溶液
- C、18.4mol/L的硫酸溶液
- D、1.0mol/L的CuSO4溶液
正确答案:A -
第22题:
单选题1L溶液中HAc的溶度为1.0mol/L,NaAc的浓度为0.1mol/L,则该溶液的PH值为()HAc的pKa=4.74。A2.74
B3.74
C4.74
D5.74
正确答案: B解析: 暂无解析 -
第23题:
单选题对于电池Zn|ZnSO4(1mol/L)‖CuSO4(1mol/L)|Cu()AZn极为正极
BZn极发生还原反应
CCu极发生还原反应
DCu极发生氧化反应
正确答案: B解析: 暂无解析

 在1.0mol/L溶液与0.5mol/L溶液中OH伸缩振动频率发生什么变化?为什么?
在1.0mol/L溶液与0.5mol/L溶液中OH伸缩振动频率发生什么变化?为什么?