标准摩尔反应焓的大小只取决于反应的始态和终态,与反应途径无关。
题目
标准摩尔反应焓的大小只取决于反应的始态和终态,与反应途径无关。
相似考题
参考答案和解析
更多“标准摩尔反应焓的大小只取决于反应的始态和终态,与反应途径无关。”相关问题
-
第1题:
下列反应中,反应的标准摩尔焓变等于产物的标准摩尔生成焓的是( )。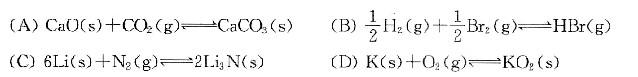 答案:D解析:标准摩尔生成焓是指标准状态下由稳定相单质生成1摩尔某相物质时反应焓。上述四个选项中只有K(s)+O2(g)→KO2(s)的反应符合要求
答案:D解析:标准摩尔生成焓是指标准状态下由稳定相单质生成1摩尔某相物质时反应焓。上述四个选项中只有K(s)+O2(g)→KO2(s)的反应符合要求 -
第2题:
关于催化剂,下列叙述错误的是()
- A、催化剂不能改变反应的始态和终态
- B、催化剂不能影响产物和反应物的相对能量
- C、催化剂不参与反应
- D、催化剂同等程度地加快正逆反应的速度
正确答案:C -
第3题:
动力学分析只涉及反应过程的始态和终态,不涉及中间过程。
正确答案:错误 -
第4题:
化学反应的热效应与物质的始态和终态无关,与变化的途径有关。
正确答案:错误 -
第5题:
由于零级反应中反应速率与浓度无关,故流体的混合态对反应结果无影响。
正确答案:错误 -
第6题:
在温度T的标准状态下,若已知反应A→2B的标准摩尔反应焓ΔrHΘm,1,与反应2A→C的标准摩尔反应焓ΔrHΘm,2,则反应C→4B的标准摩尔反应焓ΔrHΘm,4与ΔrHΘm,1及ΔrHΘm,2的关系为ΔrHΘm,3=?()
- A、2ΔrHΘm,1+ΔrHΘm,2
- B、ΔrHΘm,1-2ΔrHΘm,2
- C、ΔrHΘm,1+ΔrHΘm,2
- D、2ΔrHΘm,1-ΔrHΘm,2
正确答案:D -
第7题:
化学反应的焓变只与物质的始终态有关,而与变化途径无关。
正确答案:正确 -
第8题:
改正以下表述中的错误,给出正确表述。“把H2和O2在一定温度下混合为标准态压力下的混合气,反应生成1molH2O(g)的焓变是H2O(g)的标准摩尔生成焓ΔfH9m(H2O,g),它代表了H2O(g)的摩尔焓值。”
正确答案:不是混合成标准态压力下的混合气,因为混合过程有焓变,此值不代表H2O(g)的焓值,而是H2O(g)相对于H2(g)和O2(g)的焓的差值,正确的表述为:在一定温度下,由标准态的1molH2(g)和标准态的0.5molO2(g)反应生成标准态的1molH2O(g)的焓变是H2O(g)的标准摩尔生成焓,它是各自处于标准态下H2O(g)相对于1molH2(g)和0.5molO2(g)的焓差。 -
第9题:
过渡态理论认为反应速率与活化络合物在反应途径方向上的()频率成正比。
正确答案:不对称伸缩振动 -
第10题:
在相同的温度和压力下,一定量氢气和氧气从四种不同的途径生成水: (1)氢气在氧气中燃烧; (2)爆鸣反应; (3)氢氧热爆炸; (4)氢氧燃料电池。 在所有反应中,保持反应始态和终态都相同,请问这四种变化途径的热力学能和焓的变化值是否相同?
正确答案:应该相同。因为热力学能和焓是状态函数,只要始终态相同,无论通过什么途径,其变化值一定相同。这就是:异途同归,值变相等。 -
第11题:
单选题催化剂对化学反应速率的影响,下列描述错误的是()。A热力学上不可能发生的反应,在催化剂作用下仍可以发生反应
B催化剂只能改变反应的途径,不能改变反应的始态和终态
C催化剂有选择性,不同的反应常采用不同的催化剂
D每种催化剂往往只能在特定条件下才能体现出它的活性
正确答案: C解析: 暂无解析 -
第12题:
单选题已知298K时,Ag2O(s)的△fGθ=-10.82kJ·mol-1,则Ag2O(s)分解为Ag(s)和O2(g)的反应可能是()。A在标准状态时是非自发反应
B在标准态时是自发反应
C在室温标准态时是自发反应
D在室温标准态时是非自发反应
正确答案: A解析: △G是判断自发反应的依据,△G<0,反应为自发过程,不可逆,△G>0为非自发的反应,△G=0说明反应处于平衡状态。 -
第13题:
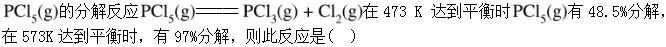 A.吸热反应;
A.吸热反应;
B.放热反应;
C.反应的标准摩尔焓变为零的反应;
D.在这两个温度下标准平衡常数相等的反应。答案:A解析: -
第14题:
关于熵和焓,以下说法正确的是()。
- A、物质的相对分子质量相近,其标准熵值相近
- B、反应过程的熵变只与始态和终态有关,与过程无关
- C、若化学反应的焓变小于0,熵变大于0,则反应必定向正方向进行
- D、热力学上298K时所有稳定单质的标准生成自由焓为零
正确答案:B,C,D -
第15题:
根据盖斯定律的含义,化学反应的热效应只与反应的()有关.
- A、温度、压力等状态因素
- B、分子的键能
- C、步骤或途径
- D、初始态和终态
正确答案:D -
第16题:
催化剂在始态时()。
- A、参与了反应
- B、不参与反应
- C、不改变反应速度
正确答案:A -
第17题:
对于热化学反应方程,表述正确的有()
- A、不同组分表示的化学反应进度相同
- B、反应进度与方程式书写无关
- C、化学反应焓变与方程式书写形式无关
- D、化学反应摩尔焓变与反应方程式书写形式无关
正确答案:A,D -
第18题:
对于盖斯定律,下列表述不正确的是()
- A、盖斯定律反应了体系从一个状态变化到另一状态的总能量变化;
- B、盖斯定律反应了体系状态变化时其焓变只与体系的始态.终态有关,而与所经历的步骤和途径无关;
- C、盖斯定律反应了体系状态变化时其熵变只与体系的始终态有关,而与所经历的步骤和途径无关;
- D、盖斯定律反应了体系状态变化时其自由能变只与体系的始终态有关,而与所经历的步骤和途径无关.
正确答案:A -
第19题:
催化剂对化学反应速率的影响,下列描述错误的是()。
- A、热力学上不可能发生的反应,在催化剂作用下仍可以发生反应
- B、催化剂只能改变反应的途径,不能改变反应的始态和终态
- C、催化剂有选择性,不同的反应常采用不同的催化剂
- D、每种催化剂往往只能在特定条件下才能体现出它的活性
正确答案:A -
第20题:
欲知绝热不可逆变化的熵变,可以通过下列哪些途径求得?()
- A、始、终态相同的可逆绝热途径
- B、始、终态相同的可逆非绝热途径
- C、始、终态相同的任何可逆途径
- D、始、终态相同的其他非可逆途径
- E、始、终态相同的一条可逆绝热途径和其他若干条可逆途径
正确答案:B,C,E -
第21题:
若规定温度T时,处于标准态的稳定态单质的标准摩尔生成焓为零,那么该温度下稳定态单质的热力学能的规定值也为零。
正确答案:错误 -
第22题:
过渡态理论对活化络合物的假设中,以下说法不正确的为:()
- A、是处在鞍点时的分子构型
- B、正逆反应的过渡态不一定相同
- C、存在着与反应物间化学平衡
- D、生成的过渡态不能返回反应始态
正确答案:B -
第23题:
判断题盖斯定律反映了体系状态变化时其焓变只与体系的始态.终态有关,而与所经历的步骤和途径无关。A对
B错
正确答案: 对解析: 暂无解析 -
第24题:
判断题化学反应的反应热只与反应的始态和终态有关,而与变化的途径无关。A对
B错
正确答案: 错解析: 暂无解析
