根据国家食品药品监督管理总局制定的化学药品新注册分类,对已知活性成分的剂型、给药途径进行优化,且具有明显临床优势的,中国境内外均未上市的药品属于A.仿制药 B.进口药品 C.创新药 D.改良型新药
题目
B.进口药品
C.创新药
D.改良型新药
相似考题
参考答案和解析
更多“根据国家食品药品监督管理总局制定的化学药品新注册分类,对已知活性成分的剂型、给药途径进行优化,且具有明显临床优势的,中国境内外均未上市的药品属于”相关问题
-
第1题:
根据《关于发布化学药品注册分类改革工作方案的公告》(国家食品药品监督管理总局2016年第51号)。境内申请人仿制境外,上市但境内未上市原研药品的药品,按新的注册分类属于( )。
A.2类
B.3类
C.5类
D.4类
正确答案:B
-
第2题:
根据国家食品药品监督管理总局关于发布化学药品注册分类改革工作方案的公告(2016年第51号),以下哪种情形属于仿制药()A.境内外均未上市的创新药
B.境内外均未上市的改良型新药
C.境外上市的药品申请在境内上市
D.仿制境外上市但境内未上市原研药品的药品
正确答案:D
-
第3题:
《药品注册管理办法》规定,应按照新药申请程序申报的是
A. 未曾在中国境内上市销售的药品的注册
B. 生产国家食品药品监督管理局已批准上市的已有国家标准的生物制品的注册
C. 已上市药品改变剂型的注册
D. 已上市药品改变给药途径的注册
E. 增加新适应症的药品的注册
正确答案:ABCDE
-
第4题:
根据国家食品药品监督管理总局制定的化学药品新注册分类对已知活性成分的基础上,对其结构、剂型、处方工艺、给药途径等进行优化,且具有明显临床优势的,境内外均未上市的药品属于A.仿制药
B.进口药品
C.创新药
D.改良型新药答案:D解析:境内外均未上市的改良型新药指在已知活性成分的基础上,对其结构、剂型、处方工艺、给药途径等进行优化,且具有明显临床优势的药品。 -
第5题:
根据《关于发布化学药品注册分类改革工作方案的公告》(国家食品药品监督管理总局2016年第51 号)境外上市的药品申请在境内上市,按新的注册分类属于A.2 类
B.3 类
C.4 类
D.5 类答案:D解析: -
第6题:
根据国家食品药品监督管理总局制定的化学药品新注册分类境内申请人仿制境外上市但境内未上市原研药品的药品属于A.仿制药
B.进口药品
C.创新药
D.改良型新药答案:A解析: -
第7题:
根据国家食品药品监督管理总局制定的化学药品新注册分类,有新的结构明确的、具有药理作用的化合物,且具有临床价值的药品属于A.仿制药
B.进口药品
C.创新药
D.改良型新药答案:C解析: -
第8题:
根据国家食品药品监督管理总局制定的化学药品新注册分类在已知活性成分的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化,且具有明显临床优势,中国境内外均未上市的药品属于A.仿制药
B.进口药品
C.创新药
D.改良型新药答案:D解析: -
第9题:
下列说法正确的是()
- A、仿制药是指生产国家食品药品监督管理局已批准上市的已有国家标准的药品
- B、对已上市药品改变剂型、改变给药途径、增加新适应证的药品注册按照仿制药申请的程序申报
- C、对境内生产的药品在境外上市销售的注册申请属进口药品申请
- D、《药品注册管理办法》在中华人民共和国境内使用仅包括药品生产和药品进口、进行药品审批、注册检验和监督管理
- E、Ⅳ期临床试验目的是观察人体对新药的耐受程度和药代动力学,为制定给药方案提供依据
正确答案:A -
第10题:
负责组织对药品注册申请进行技术审评的机构是()
- A、中国食品药品检定研究院
- B、国家食品药品监督管理总局药品审评中心
- C、国家食品药品监督管理总局药品评价中心
- D、国家食品药品监督管理总局食品药品审核查验中心
正确答案:B -
第11题:
单选题下列说法正确的是()A仿制药是指生产国家食品药品监督管理局已批准上市的已有国家标准的药品
B对已上市药品改变剂型、改变给药途径、增加新适应证的药品注册按照仿制药申请的程序申报
C对境内生产的药品在境外上市销售的注册申请属进口药品申请
D《药品注册管理办法》在中华人民共和国境内使用仅包括药品生产和药品进口、进行药品审批、注册检验和监督管理
EⅣ期临床试验目的是观察人体对新药的耐受程度和药代动力学,为制定给药方案提供依据
正确答案: A解析: 暂无解析 -
第12题:
单选题根据《关于发布化学药品注册分类改革工作方案的公告》的药品注册分类在已知活性成分的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化,且具有明显临床优势的药品注册类别是()A4类
B2类
C3类
D1类
正确答案: D解析: -
第13题:
根据《关于发布化学药品注册分类改革工作方案的公告》的药品注册分类。在已知活性成分的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化,且具有明显临床优势的药品注册类别是()A.3类
B.1类
C.4类
D.2类
参考答案:D
-
第14题:
对药品注册申请进行技术审评的机构是
A、国家药典委员会
B、国家食品药品监督管理总局信息中心
C、国家食品药品监督管理总局药品评价中心
D、国家食品药品监督管理总局药品审评中心
E、中国食品药品检定研究院
参考答案:D
-
第15题:
改变国内已上市销售药品剂型但不改变给药途径的化学药品制剂属于
A.化学药品注册分类1类
B.化学药品注册分类2类
C.化学药品注册分类3类
D.化学药品注册分类4类
E.化学药品注册分类5类
正确答案:E
解析:化学药品注册分类中,注册分类5类的新药是改变国内已上市销售药品剂型但不改变给药途径的制剂。 -
第16题:
根据国家食品药品监督管理总局制定的化学药品新注册分类有新的结构明确的、具有药理作用的化合物,且具有临床价值的药品,境内外均未上市的药品属A.仿制药
B.进口药品
C.创新药
D.改良型新药答案:C解析:境内外均未上市的创新药指含有新的结构明确的、具有药理作用的化合物,且具有临床价值的药品。 -
第17题:
根据2016年3月发布的《关于发布化学药品注册分类改革工作方案的公告》,化学药品新注册分类中按照新药程序申报的是A.境内外均未上市的创新药
B.境内外均未上市的改良型新药
C.境内申请人仿制境外上市境内未上市原研药品的药品
D.境外上市的药品申请在境内上市答案:A,B解析:AB按新药程序申请;C按仿制药的程序申请;D按进口药品的程序申请。 -
第18题:
在已知活性成分的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化,且具有明显临床优势的药品注册类别是( )A.4类
B.2类
C.3类
D.1类答案:B解析:2类:境内外均未上市的改良型新药。指在已知活性成分的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化,且具有明显临床优势的药品。 -
第19题:
根据《关于发布化学药品注册分类改革工作方案的公告》(国家食品药品监督管理总局2016年第51号),境内外均未上市的创新药,按新的注册分类属于A.1类
B.2类
C.3类
D.4类答案:A解析: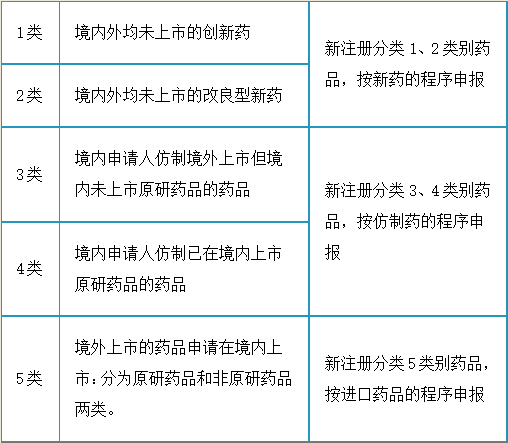
-
第20题:
根据《关于发布化学药品注册分类改革工作方案的公告》(国家食品药品监督管理总局2016年第51号),境内申请人仿制已在境内上市原研药品的药品,按新的注册分类属于A.1类
B.2类
C.3类
D.4类答案:D解析: -
第21题:
对已上市药品改变剂型但不改变给药途径的注册申请,应当采用新技术以提高药品的质量和安全性,且与原剂型比较有明显的临床应用优势。改变剂型但不改变给药途径,以及增加新适应症的注册申请,应当由具备生产条件的企业提出;靶向制剂、缓释、控释制剂等特殊剂型除外。
正确答案:正确 -
第22题:
下列属于化学药品注册三类的是()
- A、境内外均未上市的创新药
- B、境内外均未上市的改良型新药
- C、仿制境外上市但境内未上市原研药品的药品
- D、仿制境内已上市原研药品的药品
正确答案:C -
第23题:
单选题负责组织对药品注册申请进行技术审评的机构是()A中国食品药品检定研究院
B国家食品药品监督管理总局药品审评中心
C国家食品药品监督管理总局药品评价中心
D国家食品药品监督管理总局食品药品审核查验中心
正确答案: D解析: CFDA药品评价中心加挂"国家药品不良反应监测中心"牌子;CFDA食品药品审核查验中心组织开展药品注册现场核查相关工作;CFDA药品审评中心负责组织对药品注册申请进行技术审评。 -
第24题:
单选题药品注册申请分类的表述,错误的是A新药界定为国内外均未曾上市的创新药和国外已上市但未曾在我国境内上市销售的药品。
B已上市药品改变剂型、改变给药途径、增加新适应症的药品按照新药申请的程序申报。
C改剂型但不改给药途径、以及增加新适应症的注册申请获得批准后发给药品批准文号和新药证书
D未在生产国家或者地区获得上市许可,但经国家食品药品监督管理局确认该药品安全、有效而且临床需要的,可以批准进口
正确答案: B解析:
