14、浓度为 c mol/L 的一元弱碱(解离常数为 Kb)溶液中氢离子(或氢氧根)浓度计算最简式为A.[H+] = (Kb×c)^(1/2)B.[OH-] = (Kb×c)^(1/2)C.[H+] = (Kw/Kb×c)^(1/2)D.[OH-] = (Kw/Kb×c)^(1/2)
题目
14、浓度为 c mol/L 的一元弱碱(解离常数为 Kb)溶液中氢离子(或氢氧根)浓度计算最简式为
A.[H+] = (Kb×c)^(1/2)
B.[OH-] = (Kb×c)^(1/2)
C.[H+] = (Kw/Kb×c)^(1/2)
D.[OH-] = (Kw/Kb×c)^(1/2)
相似考题
更多“14、浓度为 c mol/L 的一元弱碱(解离常数为 Kb)溶液中氢离子(或氢氧根)浓度计算最简式为”相关问题
-
第1题:
某一元弱碱的共轭酸的水溶液浓度为0.1mol/L,其PH值为3.48,该弱碱的PKb的近似值应为10.04。
此题为判断题(对,错)。
正确答案:×
-
第2题:
pH=l和pH=2的溶液中,氢离子浓度之比为10:1,氢氧根离子浓度之比为()
正确答案:1:10
-
第3题:
已知某溶液的pH值为12.35,其氢离子浓度的正确值为( )mol/L。A.
B.
C.
D. 答案:C解析:pH及对数值计算,有效数字按小数点后的位数保留,pH:12.35,两位有效数字。
答案:C解析:pH及对数值计算,有效数字按小数点后的位数保留,pH:12.35,两位有效数字。 -
第4题:
pH的定义是()。
- A、溶液中氢氧根离子浓度的对数
- B、溶液中氢离子活度的对数
- C、溶液中氢离子活度的负对数
- D、溶液中氢离子浓度的对数
- E、溶液中氢离子浓度的负对数
正确答案:C -
第5题:
设弱酸HA的电离度为α,0.1mol/L溶液中的氢离子的浓度是:()
- A、αmol/L
- B、0.1αmol/L
- C、0.01αmol/L
- D、0.001αmol/L
- E、0.0001αmol/L
正确答案:B -
第6题:
NaHCO3水溶液中氢离子浓度的计算公式为(),HAc-NaAc缓冲溶液氢离子浓度的计算公式为()。
正确答案:[H+]=Ka1·K;[H+]=Ka·C酸/C盐 -
第7题:
强酸强碱在水中是()解离的。因此,一元强酸溶液的氢离子浓度()该酸的浓度;一元强碱溶液的氢氧根离子的浓度()该碱的浓度。
正确答案:完全;等于;等于 -
第8题:
某溶液的pH为10.25,该pH的有效数字为()位,其氢离子活度为()mol/L,氢氧根离子活度为()mol/L。
正确答案:=;5.6×10-11mol/L;1.8×10-4mol/L -
第9题:
弱酸或弱碱的解离平衡常数KΘ不仅与溶液温度有关,而且与其浓度有关。
正确答案:错误 -
第10题:
已知某一元弱酸的浓度为0.01mol/L,pH=4.55,则其解离常数Ka为()。
- A、5.8×10-2
- B、9.8×10-3
- C、8.6×10-7
- D、7.97×10-8
正确答案:D -
第11题:
计算0.1mol/L甲酸(甲酸的Ka=1.8x10-4)溶液的H+浓度可用最简式计算。
正确答案:正确 -
第12题:
填空题强酸强碱在水中是()解离的。因此,一元强酸溶液的氢离子浓度()该酸的浓度;一元强碱溶液的氢氧根离子的浓度()该碱的浓度。正确答案: 完全,等于,等于解析: 暂无解析 -
第13题:
浓度为0.1mol/L的某弱酸弱碱盐NH4A溶液pH=7.00,则HA的pKa为( )。
(已知:NH3·H2O的Kb=1.8×10-5)
求计算过程
答案:
NH4A在质子论当作两性物质 [H+]=约=[Ka(NH4+) *Ka(HA)]^1/2 [H+]^2 =Ka(NH4+)* Ka(HA) 而Ka(NH4+)=Kw/Kb(NH3) 因此 [H+]^2 =Kw/ Kb(NH3)* Ka(HA) (10^-7)^2=10^-14 /Kb(NH3)* Ka(HA) 即:Ka(HA)=Kb(NH3)=1.8*10^-5。
-
第14题:
已知某一元弱酸的浓度为0.01mol/L,pH=4.55,则其解离常数Ka为( )。A.
B.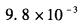
C.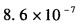
D.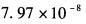 答案:D解析:
答案:D解析: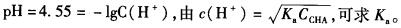
-
第15题:
0.2mol/L的HAc溶液中的氢离子浓度是0.1mol/LHAc溶液中氢离子浓度的两倍。17.
正确答案:错误 -
第16题:
浓度为0.01 mol·L–1的一元弱碱(KbΘ=1.0×10–8),其pH=()。
正确答案:9.0 -
第17题:
在H2S水溶液中,氢离子与氢氧根离子浓度乘积的对数为-14。
正确答案:正确 -
第18题:
PH=0时表示()。
- A、氢离子浓度为0
- B、纯水
- C、氢离子浓度为1mol/l
- D、溶液中无离子存在
正确答案:C -
第19题:
浓度为0.010mol·dm-3的某一元弱碱(Kbθ=1.0×10-8)溶液,其pH=(),此碱的溶液与等体积的水混和后,pH=()。
正确答案:9.0;8.85 -
第20题:
已知298K时浓度为0.010mol·L-1的某一元弱酸溶液的pH为4.00,则该酸的解离常数等于1.0*10-6;将该酸溶液稀释后,其pH将变大,解离度α将变大,其KaΘ将()。
正确答案:不变 -
第21题:
已知298K时浓度为0.010mol·L-1的某一元弱酸的pH为4.00,则该酸的解离常数为(),当把该酸溶液稀释后,其pH将变(),解离度将变(),其KaΘ()。
正确答案:1.0×10-6;大;大;不变 -
第22题:
某溶液氢离子浓度为2.5×10-3mol/L,有效数字是()位,pH为()
正确答案:=;2.60 -
第23题:
单选题pH值的定义是()A溶液中氢氧根离子浓度的对数
B溶液中氢离子活度的对数
C溶液中氢离子活度的负对数
D溶液中氢离子浓度的对数
E溶液中氢离子浓度的负对数
正确答案: D解析: 暂无解析 -
第24题:
单选题已知浓度为0.01mol/L的某一元酸溶液的pH值为5.5,则该溶液的解离常数为()。A10-10
B10-9
C10-8
D10-3
正确答案: B解析: 暂无解析
