3、用0.1000 mol/LHCl滴定0.1000 mol/LNaOH时的突跃为9.7~4.3,用0.01000 mol/LHCl滴定0.01000 mol/LNaOH时的突跃范围是A.9.7~4.3B.8.7~4.3C.9.7~5.3D.8.7~5.3
题目
3、用0.1000 mol/LHCl滴定0.1000 mol/LNaOH时的突跃为9.7~4.3,用0.01000 mol/LHCl滴定0.01000 mol/LNaOH时的突跃范围是
A.9.7~4.3
B.8.7~4.3
C.9.7~5.3
D.8.7~5.3
相似考题
更多“3、用0.1000 mol/LHCl滴定0.1000 mol/LNaOH时的突跃为9.7~4.3,用0.01000 mol/LHCl滴定0.01000 mol/LNaOH时的突跃范围是”相关问题
-
第1题:
用0.01000mol/LHNO3溶液滴定20.00mL0.01000mol/LKOH溶液的突跃范围为pH=5.3~8.7,可选用的指示剂有()。A、甲基橙
B、甲基红
C、酚酞
D、百里酚酞
参考答案:BC
-
第2题:
01mol/LHCl滴定0.01mol/LNaOH时用什么指示剂?为什么?
正确答案:酸和碱的浓度减少10倍,滴定突跃也减少2个pH单位,即5.3~8.7,不能用甲基橙,只能用甲基红。
-
第3题:
用氢氧化钠滴定液(0.1000 mol/L)滴定20.00 ml盐酸溶液(0.1000 mol/L),滴定突跃范围的pH值是
A. 1.00-3.00
B.3.00—4.30
C. 4.30-9.70
D.8.00-9.70
E. 9.70-10.00
正确答案:D本题考查酸碱突跃的范围。强碱强酸的滴定突跃为4.30~9.70。
-
第4题:
用0.10mol/LHCl溶液滴定0.10mol/LNaOH溶液,其pH值突跃范围为4.3~9.7,如果用0.010mol/LHCl溶液滴定0.010mol/LNaOH溶液,估计其突跃范围是( )。A.4.3~9.7
B.3.3~10.7
C.3.3~8.7
D.5.3~8.7答案:D解析:强酸碱相互滴定时,强酸碱浓度增大(或减少)一个数量级,则滴定突跃增大(或减少)两个pH单位。 -
第5题:
用下列四种不同浓度的NaOH标准溶液:①1.000mol/L;②0.5000mol/L;③0.1000mol/L;④0.01000mol/L。滴定相应浓度的HCl标准溶液,得到滴定曲线,其中滴定突跃最宽,可供选择的指示剂最多的是( )。A. ①
B. ②
C. ③
D. ④答案:A解析:在化学计量点前后±0.1%(滴定分析允许误差)范围内,溶液参数将发生急剧变化,这种参数(如酸碱滴定中的pH)的突然改变就是滴定突跃,突跃所在的范围称为突跃范围。突跃的大小受滴定剂浓度(c)和酸(或碱)的解离常数影响,c越大,解离常数越大,突跃越大。 -
第6题:
用0.1mol/LHCl滴定0.1mol/LNaOH时pH突跃范围是9.7~4.3,用0.01mol/LHCl滴定0.01mol/LNaOH时pH突跃范围是()。
- A、9.7~4.3
- B、8.7~4.3
- C、8.7~5.3
- D、10.7~3.3
正确答案:C -
第7题:
用0.1000 mol/L的HCL溶液滴定等浓度NaOH的pH突跃范围为9.7~4.3。若浓度减小10倍,则pH突跃范围为()。
正确答案:8.7-5.3 -
第8题:
用0.1000mol/LNaOH滴定0.1000mol/LHAc时指示剂应选()。
- A、甲基橙
- B、溴酚蓝
- C、甲基红
- D、酚酞
正确答案:D -
第9题:
用0.1mol/L NaOH滴定HAc的突跃范围为7.7~9.7,则用0.01mol/L NaOH滴定HAc的突跃范围6.7~8.7。
正确答案:错误 -
第10题:
用0.2mol/ LHCl溶液滴定0.10mol/L NH3(pKb=4.74)和甲胺(pKb=3.38)的混合溶液时,在滴定曲线上,出现()个滴定突跃。
正确答案:1 -
第11题:
用0.1000mol/LNaOH滴定25.00mL0.1000mol/LHCl,若以甲基橙为指示剂滴定至pH=4.0为终点,其终点误差Et=()%。
正确答案:-0.2% -
第12题:
单选题用0.1mol/L HCl滴定0.1mol/L NaOH的突跃范围为9.7~4.3,则0.01mol/L HCl滴定0.01mol/L NaOH的突跃范围应为()A9.7~4.3
B8.7~4.3
C8.7~5.3
D10.7~3.3
正确答案: D解析: 暂无解析 -
第13题:
用氢氧化钠滴定液(0.1000mol/L)滴定20.00ml盐酸溶液(0.1000mol/L),滴定突跃范围的pH是( )
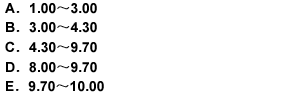 正确答案:C
正确答案:C
-
第14题:
用NaOH滴定液(0.1000mol/L)滴定20.00ml盐酸溶液(0.1000mol/L)时,其滴定突跃的pH范围为( )
A.7.74~9.70
B.5.3~8.7
C.4.3~9.7
D.3.3~10.7
E.6.24~4.30
正确答案:C
-
第15题:
用0.1000mol/LHCl溶液滴定25.00mlNaOH溶液,终点时消耗20.00ml,则NaOH溶液的浓度为( )A.0.1000mol/L
B.0.8000mol/L
C.0.08mol/L
D.0.08000mol/L
E.0.1250mol/L答案:D解析: -
第16题:
用下列四种不同浓度的NaOH标准溶液①1.000mol/L;②0.5000mol/L;③0.1000mol/L;④0.01000mol/L滴定相应浓度的HCl标准溶液,得到四条滴定曲线,其中滴定突跃最宽,可供选择的指示剂最多的是( )。A.①
B.②
C.⑧
D.④答案:A解析:分析化学中,在化学计量点前后±0.1%(滴定分析允许误差)范围内,溶液参数将发生急剧变化,这种参数(如酸碱滴定中pH)的突然改变就是滴定突跃,突跃所在的范围称为突跃范围。突跃的大小受滴定剂浓度(c)和酸(或碱)的解离常数影响,c越大,突跃越大,解离常数越大,突跃越大。 -
第17题:
用0.1mol/L HCL滴定0.1mol/L NaOH时的pH突跃范围是9.7~4.3,用0.01mol/L HCl滴定0.01mol/L NaOH时的pH突跃范围是()。
- A、10.7~3.3
- B、8.7~4.3
- C、9.7~4.3
- D、8.7~5.3
正确答案:D -
第18题:
用0.01000mol/LHN03溶液滴定20.00mL0.01000mol/LKOH溶液的突跃范围为pH:5.3-8.7,可选用的指示剂有()。
- A、甲基橙
- B、甲基红
- C、酚酞
- D、百里酚酞
正确答案:B,C -
第19题:
0.1mol/lHCl滴定0.1mol/lNaOH时(以其化学式为基本单元),pH突跃范围是9.7~4.3,用1mol/lHCl滴定1mol/lNaOH时pH突跃范围应为()。
- A、9.7~4.3
- B、8.7~4.3
- C、9.7~5.3
- D、8.7~5.3
- E、10.7~3.3
正确答案:E -
第20题:
用0.10mol/LHCL溶液滴定0.10mol/LNaOH溶液,其PH突跃范围为9.7~4.3,如果改用0.010mol/LHCL溶液滴定0.010mol/LNaOH溶液,估计其突跃范围是()。
- A、9.7~4.3
- B、10.7~3.3
- C、8.7~3.3
- D、8.7~5.3
正确答案:D -
第21题:
用0.1mol/L HCl滴定0.1mol/L NaOH的突跃范围为9.7~4.3,则0.01mol/L HCl滴定0.01mol/L NaOH的突跃范围应为()
- A、9.7~4.3
- B、8.7~4.3
- C、8.7~5.3
- D、10.7~3.3
正确答案:C -
第22题:
以0.1000mol/LHCl溶液滴定20.00mL0.1000mol/LNH3(Kb=1.8x10-5)溶液,计算滴定前,滴定突跃范围(滴定误差在0.1%范围)及化学计量点的pH值。
正确答案: 滴定前0.1000mol/LNH3溶液,c/Kb>100,cKb>10Kw
可用最简式[OH-]=(cKb)1/2=1.30x10-5mol/L,pOH=2.89pH=11.11
滴定误差-0.1%,加入HCl19.98mL时
因为HCl的滴入,溶液为NH3及其共轭酸NH4+组成的缓冲溶液,
pH=pKb+lg[Ac-]/[HAc]=4.74+lg(0.02/19.98)=6.30
滴定误差+0.1%,加入NaOH20.02mL时,HCl过量,
[H+]=(20.02-20.00)/(20.02+20.00)=5.00x10-5mol/L,pOH=4.30,pH=4.30
滴定突跃范围:6.30~4.30
化学计量点,HCl和NH3定量反应全部生成NH4Cl,又因溶液的体积增大1倍,
故:CNH4+=0.0500mol/L,此时溶液的酸度主要由NH4+的解离所决定。
Ka=Kw/Kb=5.6x10-10,c/Ka>100,cKa>10Kw,
所以[H+]=(cKa)1/2=(0.0500x5.6x10-10)1/2=5.3x10-6mol/L,pH=5.28 -
第23题:
下列滴定中,不能准确滴定的是()
- A、0.10mol/LHCl滴定0.10mol/LNH3•H2O(KB=1.75×10-5)
- B、0.10mol/LNAOH滴定0.10mol/LNH4Cl
- C、0.10mol/LHCl滴定0.10mol/LNACN(KA=4.9×10-10)
- D、0.10mol/LNAOH滴定0.10mol/LHCOOH(KA=1.7×10-4)
正确答案:B -
第24题:
单选题用0.10mol/LHCL溶液滴定0.10mol/LNaOH溶液,其PH突跃范围为9.7~4.3,如果改用0.010mol/LHCL溶液滴定0.010mol/LNaOH溶液,估计其突跃范围是()。A9.7~4.3
B10.7~3.3
C8.7~3.3
D8.7~5.3
正确答案: A解析: 暂无解析
