安徽省学年阜阳市颍上县第二中学高一月月考化学试题
可能用到的相对原子质量:H 1 C 12 0 16 Na 23 Mg 24 Al 27 Cl 35.5
1.(2009?重庆)下列变化中属于化学变化的是( )
A.木柴劈成块 B.西瓜榨成汁 C.残雪化成水 D.高粱酿成酒
有以下程序
#include <stdio.h>
int fun(int (*s)[4],int n, int k)
{ int m,i;
m=s[0][k];
for(i=1;i<n;i++) if(s[i][k]>m)m= s[i][k];
return m;
}
main()
{ int a[4][4]={{1,2,3,4},{11,12,13,14},{21,22,23,24},{31,32,33,34}};
printf("%d\n",fun(a,4,0));
}
程序的运行结果是
A)4
B)34
C)31
D)32

可能用到的相对原子质量H—1 C—12 O—16 Mg—24 Cl—36.5
1、 日常生活中发生的下列变化,属于化学变化的是( )
A. 水结成冰 B。纸张燃烧 C 玻璃破碎 D 汽油挥发
可能用到的相对原子质量:H—1,C—12,N—14,O—16,Na—23,Mg—24,Al—27,S—32,Cl—35.5,Ca—40,Fe—56,Zn—65,Ag—108
1.下列变化中属于化学变化的是
A.榨取果汁 B.粉碎废纸 C.燃放烟花 D.切割玻璃
可能用到的相对原子质量:H—1 C—12 N—1 O—16 Na—23 Cl—35.5 Ca—40
1.为加快建成“资源节约型城市”,苏州市推出多项措施,其中不属于“节能减排”的是
A.禁止生产、设计和使用粘土实心砖,以节约土壤资源
B.“龙芯”绿色节能电脑引入苏州常熟百所学校
C.加拿大太阳能有限公司将在苏州新区安装太阳能发电设备
D.优先大力发展城市公共交通,以减少小轿车尾气排放
安徽省颍上第二中学2019年6月月考高一化学试题 时间:90分钟 满分:100分可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32 K:39 Fe:56 Cl:35.5第I卷(选择题,共48分)一选择题(每小题只有一个选项符合题意,每小题3分,共48分)1.化学实验设计和操作中必须十分重视安全问题和环境保护问题。下列实验问题处理方法不正确的是( ) 检验CO的纯度,简单方法是用排空气法先收集一试管气体,点燃,听爆鸣声 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室。 给试管中的液体加热,不时移动试管或加入碎瓷片,以免暴沸伤人。 不慎将少量浓硫酸溅到皮肤上,应立即用大量水冲洗,然后涂稀小苏打溶液。 配制稀硫酸时,应将浓硫酸沿烧杯内壁慢慢加入到盛水的烧杯中,边加边搅拌。A. B. C. D. 2有Ca(OH)2(固体)、CuSO45H2O(固体)、CH3COOH(液态)这些物质归为一类,下列哪些物质还可以和它们归为一类 ( )A医用酒精 BFe(OH)3胶体 C液态HCl D碱石灰3 “纳米材料”是粒子直径为1 nm100nm(1nm=10-9m)的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质是溶液 是胶体 能产生丁达尔效应 能透过滤纸 不能透过半透膜 静置后,会析出黑色沉淀以上说法正确的是( )ABCD4有下列实验操作或事故处理方法正确的有:( )来源:Z+xx+k.ComA给试管中的液体加热时,应将试管倾斜,试管口斜向上,与桌面成45角,直接集中在药品处加热;B夜间发生厨房煤气泄漏,应立即开灯检查煤气泄漏的原因,并打开所有门窗通风;C用50 mL量筒量取2 mL蒸馏水;D固体药品用广口瓶保存。5为了除去粗盐中的Ca2、Mg2、SO及泥沙,得到纯净的NaCl,可将粗盐溶于水,在下列操作中选取必要的步骤和正确的操作顺序( )过滤 加过量的NaOH溶液 加过量的盐酸 加过量的Na2CO3溶液加过量的BaCl2溶液 加热蒸发A B C D6NA表示阿伏加德罗常数,下列叙述正确的是()A1 molL1Na2SO4溶液含有2NA个NaB1.7 g H2O2中含有的电子数为0.9NAC标准状况下,用H2O2制备11.2 L氧气共转移2NA个电子D等质量的N2和CO所含分子数均为NA 7在三个密闭容器中分别充入N2、H2、HCl三种气体,当它们的温度和压强都相同时,这三种气体的密度,从大到小的顺序是()A. (N2)(H2)(HCl) B. (H2)(N2)(HCl)C. (H2)(HCl)(N2) D. (HCl)(N2)(H2)8下列离子方程式书写错误的是 ( ) A、铝粉投入到NaOH溶液中:2Al+2OH-= 2AlO2-+H2B、Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-= AlO2-+2H2OC、Ca(OH)2溶液中通入足量的CO2:CO2+OH= HCO3D、Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-= 2AlO2-+H2O9水溶液中能大量共存的一组离子是()A. NH 、Ba2、Br、CO B. Cl、SO、Fe2、HC. K、Na、SO、MnO D. Na、H、NO、HCO10. 现有24 mL浓度为0.05 molL1的Na2SO3溶液恰好与20 mL浓度为0.02 molL1的K2Cr2O7溶液完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为()A.2 B.3 C.4 D.511.将等物质的量的镁和铝混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是()A.3 molL1 HCl B.4 molL1 HNO3C.8 molL1 NaOH D.18 molL1 H2SO412已知X和Y是两种单质,它们之间能发生反应:X+Y=X2+Y2。下列叙述中正确的是( )X被氧化 X是氧化剂 Y2是还原产物 X2+具有氧化性 Y2具有还原性 Y单质氧化性比X2+氧化性强ABCD13若50 g密度为 gcm3的硝酸铁溶液里含2.8 g 铁离子,则硝酸根离子的物质的量浓度是( )A/3 molL1 B15/ molL1 C1.5 molL1 D3 molL114镁、铝、铜三种金属粉末混合物, 加入过量盐酸充分反应, 过滤后向滤液中加入过量烧碱溶液, 再过滤, 滤液中存在的离子有( )A BCu2+ CAl3+ DMg2+15. 取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,同温同压下放出相同体积的气体,则两份铝片的质量之比为( )A1:1 B2:3 C3:2 D1:616现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如下图所示。原溶液中Cl与SO的物质的量之比为()A.13 B.23 C.61 D.31第II卷(非选择题,共52分)二填空题17、(10分)如下图所示是中学化学中常用的混合物分离和提纯的装置。请根据装置A、B、C、D回答下列问题:(1)从硫酸钡和硫酸钠的混合液中分离出硫酸钡,可选择装置_(填字母,下同);(2)分离酒精和水,选择装置_;来源:学科网(3)装置A中的名称是_,冷却水的流动方向是_。(4)碘水中提取碘单质(固体)的方法是:先用_装置,可选用哪种萃取剂_(填代号)然后用_装置,分离出的碘单质(固体)处于_装置中(填名称)。酒精 苯 醋酸 汽油(5)在用装置B进行操作时,为使液体顺利滴下,应进行的具体操作是_。分液后漏斗内剩余的液体从分液漏斗的_(填“上口”或“下口”)倒入烧杯。18、(8分) 二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:方法一:2NaClO3 + 4HCl 2 ClO2+ Cl2 + 2NaCl + 2H2O方法二:2NaClO3 + H2O2 + H2SO4 2 ClO2 + O2 + Na2SO4 + 2H2O(1) 方法一的离子方程式:_
可能用到的数据和资料:相对原子质量:H~1 C~12 O~16Fe~56
1.空气中含量较多且化学性质不活泼的气体是
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
有下列程序:
include<stdi0.h>
intfun(int(*s)[4],intn,intk)
{intm,i;
m=s[O][k];
for(i=1;i<n;i++)if(s[i][k]>m)m=s[i]
[k];
returnm;
}
voidmain( )
{inta[4][4]=({1,2,3,4),{11,12,13,14},{21,
22,23,24},{31,32,33,34)};
printf(”%d\n”,fun(a,4,O));
}
程序的运行结果是( )。
A.4
B.34
C.31
D.32
C。【解析】在程序中fun函数的功能在于求取三维数组S中1至n行中每行第k个元素中的最大者。注意:i=0时为第一行,故fun(a,4,O)在于求取11、21、31中的最大值,显然为31。
对于n个元素的关键字序列{k1,k2,…,kn},当且仅当满足关系ki≤k2i,且ki≤k2i+1(2i≤ n,2i+1≤n)称其为小根堆,反之则为大根堆。以下序列中,(56)不符合堆的定义。
A.(4,10,15,72,39,23,18)
B.(58,27,36,12,8,23,9)
C.(4,10,18,72,39,23,15)
D.(58,36,27,12,8,23,9)
解析:本题考查堆的概念。将序列中的元素放入一棵完全二叉树,如下所示,以便于观察结点 ki,k2i和ki、k2i+1(2i≤n,2i+1≤n)之间的关系。
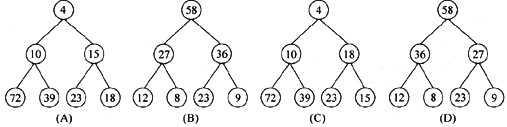
按照小根堆的定义检查选项A和C,按照大根堆的定义检查选项B和D,显然,选项C不符合小根堆的定义。
配制0.1000mg/ml磷标准溶液1000ml,需称磷酸氢二钾(KH2PO4)多少克?(已知K的相对原子质量为K=39,氢H=1,氧O=16,磷P=31)
有以下程序 #include <stdio.h> int fun(int (*s)[4],int n,int k) {int m,i; m=s[0][kl; for(i=1;i<n;i++) if(s[i][k]>m) m=s[i][k]; return m; } main() { int a[4][4]={{1,2,3,4},{11,12,13,14}, {21,22,23,24}, {31,32,33,34}}; printf("%d\n",fun(a,4,0)); } 程序的运行结果是______。
A.4
B.34
C.31
D.32
解析:在主函数中,定义并初始化了4行4列的二维数组a,并通过调用fun函数,将fun函数中指向一维数组的指针变量s指向了二维数组a的首地址,使得指针变量s与数组a共用同一存储单元。在fun函数中,通过for循环,求得了数组a第0列中最大的值,并赋给m返回主函数。由于数组a第0列的值分别为1、11、21、31,故其最大值是31。
