某溶液中含有0.010 mol/L的Fe3+和0.010 mol/L的Mg2+,已知Fe(OH)3和Mg(OH)2的Ksp分别为2.79×10-39和5.61×10-12。计算用形成氢氧化物的方法分离两种离子的pH范围。
题目
某溶液中含有0.010 mol/L的Fe3+和0.010 mol/L的Mg2+,已知Fe(OH)3和Mg(OH)2的Ksp分别为2.79×10-39和5.61×10-12。计算用形成氢氧化物的方法分离两种离子的pH范围。
相似考题
更多“某溶液中含有0.010 mol/L的Fe3+和0.010 mol/L的Mg2+,已知Fe(OH)3和Mg(OH)2的Ksp分别为2.79×10-39和5.61×10-12。计算用形成氢氧化物的方法分离两种离子的pH范围。”相关问题
-
第1题:
当Ag+、Al3+共存离子溶液各为0.010mol/L时,选择()试剂可将两种离子分离。A、1.0mol/LHCl
B、0.50mol/LH2SO4
C、0.05mol/LNH3H2O
D、2.0mol/LNaOH
E、0.02mol/LEDTA
F、1.0mol/LHNO3
G、0.50mol/LNa2S
参考答案:ACD
-
第2题:
试计算0.10mol•L-1Fe3+开始沉淀和沉淀完全时溶液的pH值。(已知Fe(OH)3的KSP=1.1×10-36)参考答案:
-
第3题:
室温下,下列溶液中的C(OH-)最小的是( )A.pH=0的溶液
B.5 mol/L HCl溶液
C.05 mol/L H2SO4溶液
D.05 mol/L Ba(OH)2溶液答案:A解析:室温下,即c(H+)·c(OH-)=1×10-14(mol/L)2.由此,c(H+)和c(OH-)只要知道其中一个即可求得另一个. A选项为pH=0的溶液,即c(H+)=1 mol/L,所以c(OH-)=1×10-14 mol/L.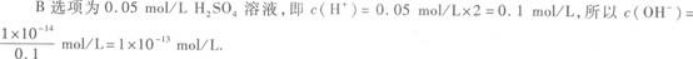
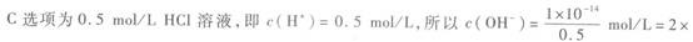
D选项为0.05 mol/L Ba(OH)2溶液,c(OH-)=0.05 mol/L×2=0.1 mol/L.
所以,c(OH-)最小的是1×10-14 mol/L,即A选项. -
第4题:
已知(Cr(OH)3)=6.3×10–31,反应Cr(OH)3+OH===[Cr(OH)4]-的平衡常数KΘ=0.40。 (1)计算Cr3+沉淀完全时溶液的pH值; (2)若将0.1mol·L–1Cr(OH)3刚好溶解在1.0LNaOH溶液中,则NaOH溶液的初浓度至少为多少? (3)计算[Cr(OH)4]-的标准稳定常数。
正确答案: (1)pH=5.60
(2)c(OH-)=0.35 mol·L–1
(3)KfΘ([Cr(OH)4]-)=6.3×1029。 -
第5题:
已知KbΘ(NH3·H2O)=1.8×10–5,在含有0.010mol·L–1 NH3·H2O和0.010 mol·L–1 KOH混合液中,c(NH4+)等于()
- A、9.0×10–4 mol·L–1
- B、1.8×10–5 mol·L–1
- C、0.020 mol·L–1
- D、6.0×10–4mol·L–1
正确答案:B -
第6题:
已知φθFe3+/Fe2+=0.77V,当溶液中[Fe3+]=0.0001mol/l,[Fe2+]=0.1000mol/l时,则半反应Fe3++e=Fe2+电极电位φFe3+/Fe2+=()。
正确答案:0.59 -
第7题:
难溶化合物Fe(OH)3离子积的表达式为()。
- A、KSP=[Fe3+][OH–]
- B、KSP=[Fe3+][3OH–]
- C、KSP=[Fe3+][3OH–]3
- D、KSP=[Fe3+][OH–]3
正确答案:D -
第8题:
已知Fe3++e=Fe2+的φΘ=0.770V,在101325Pa和298.15K时,所测得电对Fe3+/Fe2+的φ=0.750V,则该电极溶液中离子浓度必定是()
- A、[Fe3+] > 1 mol.L-1
- B、[Fe3+] < 1 mol.L-1
- C、[Fe3+]/[ Fe2+] < 1
- D、[Fe3+]/[ Fe2+] > 1
正确答案:C -
第9题:
下列溶液中,pH最小的是()
- A、0.010mol·L-1HCl;
- B、0.010mol·L-1H2SO4;
- C、0.010mol·L-1HAc;
- D、0.010mol·L-1H2C2O4。
正确答案:B -
第10题:
在某混合溶液中Fe3+和Zn2+浓度均为0.010mol·L-1。加碱调节pH,使Fe(OH)3沉淀出来,而Zn2+保留在溶液中。通过计算确定分离Fe3+和Zn2+的pH范围是()。
正确答案:2.82~6.74 -
第11题:
溶液中含有浓度均为0.010mol·L-1的Pb2+、Bi3+两种离子,问()(能/否)利用控制酸度的方法单独滴定Bi3+,而Pb2+不干扰。
正确答案:能 -
第12题:
单选题在一定温度下,能使Mg(OH)2、Fe(OH)2、Mn(OH)2等难溶物同时溶解的溶剂是( )。A1mol·L-1NH3·H2O
B纯H2O
C1mol·L-1NH4Cl
D1mol·L-1NaOH
正确答案: B解析:
B项,在一定温度下,难溶物在纯水中的溶解度为一定值;AD两项,氨水溶液中由于氨水的电离,溶液中存在OH-,溶液中的OH-不会使三种难溶物溶解,还会发生同离子效应使溶解度下降。NH4Cl可与三种不太难溶的氢氧化物生成弱电解质NH3·H2O,使OH-离子浓度下降,电离平衡右移,使沉淀Mg(OH)2、Fe(OH)2、Mn(OH)2溶解。 -
第13题:
Fe3+、Ni2+共存溶液各为0.010mol/L时,选择()试剂可将两种离子分离。A、1.0mol/LHCl
B、1.0mol/LNa2S2O3
C、0.50mol/LNH3H2O
D、2.0mol/LNaOH
E、2.0mol/LNaF
F、1.0mol/LHNO3
G、0.10mol/LH2S
参考答案:CE
-
第14题:
Mg(OH)2 在下列溶液或溶剂中的溶解度最小的是()A.0.010mol·L-1NH3溶液
B.0.010mol·L-1NaOH 溶液
C.0.010mol·L-1MgCl2溶液
D.0.010mol·L-1NH4Cl 溶液
参考答案:B
-
第15题:
已知 Ksp [Mg(OH)2] =5×10-12,现将等体积的 0.1mol/L。Mg+2溶液和 0.1mol/L NaOH溶液混合,则( )。
A.有沉淀析出 B.形成饱和溶液 C.溶液未饱和 D.无法判断答案:A解析:
-
第16题:
已知Ksp[Mn(OH)2]=2.06×10-13,Kb(NH3)=1.79×10-5。在0.200mol•L-1MnCl2100mL溶液中,加入含有NH4Cl的0.100mol•L-1NH3•H2O溶液100mL,为了不使Mn(OH)2沉淀形成,NH4Cl的物质的量应不少于()
- A、0.0662mol
- B、0.124mol
- C、0.176mol
- D、0.353mol
正确答案:B -
第17题:
298K时,Mg(OH)2在水中溶解度(mol·L-1)[已知Mg(OH)2的Ksp为5.61×10-12]是()。
- A、1.77×10-4
- B、1.12×10-4
- C、2.36×10-6
- D、1.12×10-6
正确答案:B -
第18题:
计算题:当PH=10时,溶液中〔H+〕和〔OH-〕各多少mol/L?
正确答案: 解:PH=10,即-lg〔H+〕=10
∴〔H+〕=10-10mol/L
pOH=14-PH=14-10=4
则〔OH-〕=10-4mol/L -
第19题:
以EDTA滴定浓度各为0.01mol·L-1的Fe3+和Fe2+溶液时所允许的最高酸度(最低pH)分别是()、()。
正确答案:pH=1.3;pH=5.2 -
第20题:
某溶液中含有KCl、KBr和K2CrO4,浓度均为0.010mol.L-1向溶液中逐滴加入0.1 mol.L-1AgNO3溶液时,最先和最后沉淀的是()
- A、AgBr和Ag2Cr2O4
- B、Ag2CrO4和AgCl
- C、AgCl和AgBr
- D、AgCl和Ag2CrO4
正确答案:A -
第21题:
将等体积的0.20mol·L-1的MgCl2溶液与浓度为4.0mol·L-1的氨水混合,混合后溶液中c(Mg2+)为混合前浓度的多少倍(已知K(Mg(OH)2=5.1×10-12)()
- A、1.54×10-3
- B、9.7×10-4
- C、1.54×10-4
- D、6.86×10-4
正确答案:B -
第22题:
Mg(OH)2与MnCO3的KspΘ分别为5.61×10-12和2.2×10-11,在它们的饱和溶液中[Mn2+]比[Mg2+]()。
正确答案:小 -
第23题:
当pH=10.0,以0.010mol/L EDTA溶液滴定0.010mol/LZn2+的溶液两份,其中一份溶液中含有0.5mol/L游离NH3;另一份溶液中含有0.2mol/L游离NH3。在上述两种情况下,对pZn的叙述正确的是()
- A、加入EDTA开始滴定时pZn相等
- B、滴定至一半时pZn相等
- C、滴定至化学计量点时pZn相等
- D、上述说法都不正确
正确答案:D -
第24题:
单选题用Ca(OH)2处理含Cd2+废水,欲将C蠢抖降至0.1mg/L,需保证的pH值以及此时的Ca2+浓度分别为()。(已知Cd的原子量为112,KCd(OH2)=.2×10-14)A8.7mol/L、1.1×10-6mol/L
B8.7mol/L、2.5×10-6mol/L
C9.2mol/L、1.1×10-6mol/L
D9.2mol/L、2.5×10-6mol/L
正确答案: B解析: 暂无解析
